Лоренцо Романо Амедео Карло Авогадро (1776-1856) был итальянским химиком, который первым сформулировал идею о том, что образец элемента с массой в граммах, численно равной его атомной массе, всегда имеет одинаковое количество атомов (N).
Сам Авогадро не смог определить стоимость Н. Однако на протяжении двадцатого века развитие технологий и научных знаний позволило другим ученым разработать методы для его определения. Когда это значение было наконец обнаружено, оно было названо Постоянная Авогадро, в честь этого ученого, ведь именно он заложил основы его создания.

Лоренцо Романо Амедео Карло Авогадро (1776-1856)
В 1 моль любого объекта (атомов, молекул, электронов, формул или ионов) содержится ровно значение постоянной Авогадро.
В таблице ниже показаны некоторые значения постоянной Авогадро, полученные на протяжении ХХ века:
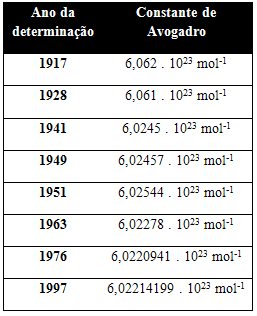
Вот некоторые из методов, используемых для определения значения постоянной Авогадро:
Первым ученым, сделавшим приблизительный расчет постоянной Авогадро, был Иоганн Йозеф Лошмидт. В 1867 году он основывался на кинетической теории газов и определил, сколько молекул существует в 1 см.
3 газа.Другим из этих ученых был француз Жан Батист Перрен (1870-1942), который подсчитал количество коллоидных частиц в единице объема суспензии и измерил их массы. Он нашел значение от 6,5 до 7,2. 1023 сущностей на моль. Этот ученый опубликовал в 1913 году книгу Les Atomes (1-е изд. Paris: Alcan), и его 9-е издание, опубликованное в 1924 году, содержало 16 способов экспериментального получения постоянной Авогадро.

Жан Батист Перрен (1870-1942)
Спустя годы ученый Джеймс Дьюар (1842-1923) использовал метод, разработанный несколькими годами ранее радиохимиком Бертрамом Болтвудом (1870-1927) и физиком Эрнестом. Резерфорда (1871-1937), который в основном состоял из подсчета альфа-частиц, испускаемых радиоактивным источником, и определения объема полученного газообразного гелия. Значение, найденное Дьюаром, составило 6,04. 1023 моль-1.
Еще в 20 веке Роберт Милликен (1868-1953) провел эксперимент по определению заряда электрона (1.6. 10-19 Ç). Поскольку заряд 1 моля электронов уже был известен (96500 Кл), можно было связать эти два значения и найти следующее значение для постоянной Авогадро: 6,03. 1023 моль-1.
В настоящее время рекомендуемое значение постоянной Авогадро составляет 6.02214 х 1023 моль-1 и он определяется посредством дифракции рентгеновских лучей, при которой получается объем нескольких атомов кристаллической решетки, если известны плотность и масса 1 моля атомов в образце.
В дидактических целях в средней школе, где вычисления не должны быть такими же точными, как в химических лабораториях, постоянная Авогадро считается равной 6,02. 1023 моль-1.
Существуют также более простые методы, которые можно использовать, чтобы помочь студентам определить константу Авогадро на практике. Один из них - путем электролиза в водной среде.
Дженнифер Фогача
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/determinacao-constante-avogadro.htm
