химический элемент фосфор (P) принадлежит к третьему периоду Периодической таблицы и к семейству азота (VA). По этой причине его атомы обычно составляют три химические связи достичь теория октетов (стабильность). Однако есть некоторые ситуации, в которых атом фосфора образует более трех связей, что возможно только через явление гибридизации.
Чтобы понять гибридизация фосфора, мы должны сначала понять, почему атом этого элемента образует три связи. Для этого нам просто нужно следить за вашей электронной рассылкой:

Электронное распределение фосфора
Мы можем наблюдать, что в валентном слое атом фосфора имеет полный 3s-подуровень (с два электрона) и неполный 3p-подуровень (каждая из трех p-подуровневых орбиталей имеет электрон). Ниже представлено распределение электронов по орбиталям подуровней Валентный слой фосфора:
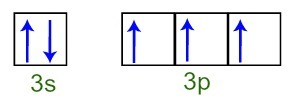
Представление электронов валентной оболочки атома фосфора
Поскольку каждая из 3p подуровневых орбиталей является неполной, атом фосфора может образовывать три химические связи, таким образом достигая стабильности.
Теперь, когда мы смотрим на вещество PCl5Например, мы уверены, что в этой молекуле фосфор подвергся гибридизации, так как образовал пять связей. Поскольку хлор, который принадлежит к семейству VIIA, нуждается в связи, чтобы быть стабильным, молекула имеет пять атомов этого элемент, каждый из них должен образовывать связь, что заставляет атом фосфора, в свою очередь, также составлять пять Связи. Это возможно только через гибридизация (объединение неполных атомных орбиталей) фосфора.
Получая энергию из внешней среды, электроны атома фосфора возбуждаются. Вскоре после этого один из двух электронов, принадлежащих подуровню 3s, перемещается на пустую орбиталь, присутствующую на подуровне d, который до этого момента не имеет электронов. См. Схему ниже:
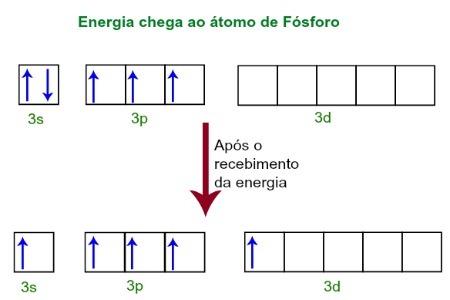
Получив энергию, электроны люминофора возбуждаются, и каждый занимает орбиталь d подуровня.
На данный момент у нас есть в валентном слое Phosphorus s-орбиталь, три p-орбитали и неполная d-орбиталь.В конечном итоге эти пять орбиталей гибридизуются, то есть сливаются, в результате чего образуются пять неполных атомных орбиталей, которые теперь способны образовывать пять химических связей.

Гибридизация неполных атомных орбиталей фосфора
Поскольку s-орбиталь, три p-орбитали и d-орбиталь были объединены, гибридизация Phosphorus имеет тип зр3d.
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm