Электролиз воды состоит из разложения этого вещества под действием электрического тока и добавления электролита. Давайте лучше разберемся, как это происходит?
Тоже читай: Что такое электролиз?
Как происходит электролиз воды?
Молекулы воды способны к самоионизации, генерируя ионы H.+ (или H3O+) и ой-:
ЧАС2O ↔ H+ + ОН-
или же
2 часа2O ↔ H3O+ + ОН-
Тем не мение, вода - очень слабый электролит и, несмотря на наличие этих ионов, он не может проводить электрический ток. Таким образом, чтобы провести его электролиз, то есть его разложение с помощью электрического тока, необходимо добавить электролит, ионное растворенное вещество, которое может быть солью, основанием или кислотой.

Приоритетный заказ на выборочную выписку
Однако, как объясняется в тексте Водный электролиз, в этом случае мы будем иметь не только ионы, поступающие из воды, но также ионы вещества, которое было в ней растворено. При электролизе на электроде разряжается только один катион и один анион, т.е. выборочная разрядка в порядке приоритета.
Таким образом, чтобы катод и анод, которые будут разряжаться, принадлежали воде, а не растворенному веществу, необходимо выбрать кислота, основание или соль, ионы которых менее легко отделяются от электродов, чем ионы в воде. Для этого нам нужно обратиться к очереди приоритетов, показанной ниже:
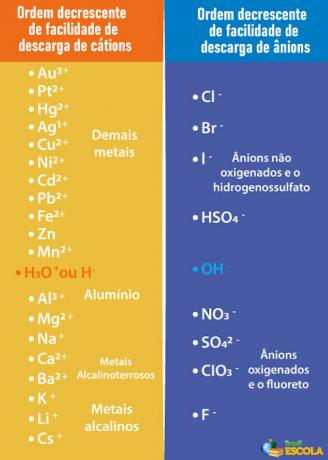
Обратите внимание, что катионы, перечисленные ниже H+ иметь меньшую легкость разгрузки, чем он. В таблице справа мы видим, что анионы ниже OH- имеют меньшую легкость разгрузки. Следовательно, мы можем выбрать, например, соль, основание или кислоту, которая образует ионы Na.+, К+, НА3-, ТОЛЬКО42- и так далее, помимо образования тех же ионов, что и вода, то есть H+ и ох-. Вот несколько примеров: серная кислота (ЧАС2ТОЛЬКО4), гидроксид натрия (NaOH) и нитрат калия (KNO3).
Пример с реакциями, происходящими при электролизе воды.
Допустим, электролиз воды проводится с добавлением серной кислоты. В этом случае в середине будет образование следующих ионов:
Кислотная диссоциация: 1 ч.2ТОЛЬКО4 → 2 H+ + 1 СО42-
Автоионизация воды: H2O → H+ + ОН- или 2 часа2O → H3O+ + ОН-
Обратите внимание, что единственный существующий катион - это H.+, значит, именно он пострадает от снижения (прироста электроны) на отрицательном электроде (катоде) и будет выделять водород.О (ЧАС2).
Теперь, говоря об анионах, есть два аниона посередине, которые являются ОС42- и ох-. Как показано в таблице выше, ОС42- он более реактивный и его труднее разряжать. Таким образом, OH- будет разряжаться, окисляясь (теряя электроны) в положительном электроде (аноде) и выделяя газ кислород(O2):
Катодная полуреакция: 4 H3O+ + 4 и- → H2O + H2
Анодная полуреакция: 4 OH- → 2 H2O + 1 O2 + 4 и-
Сложив весь этот процесс, мы приходим к глобальному уравнению:
Ионизация воды: 8 ч2O → 4 H3O+ + 4 ОН-
Катодная полуреакция: 4 H3O+ + 4 и- → 4 H2O + 2 H2
Анодная полуреакция: 4 OH- → 2 H2O + 1 O2 + 4 и-
Глобальное уравнение: 2H2O → 2 H2 + 1 O2
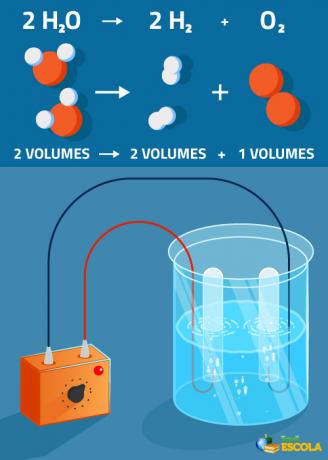
Обратите внимание, что объем производимого водорода в два раза больше, чем кислорода. Однако на практике это строгое соотношение не проверяется, потому что кислород более растворим, чем газ. водород.
Читайте тоже: Получение алюминия электролизом
Применение электролиза воды
Электролиз воды - очень важный процесс, учитывая, что водород - это газ, который можно использовать в качестве топлива. Как топливо из нефти не возобновляемы, водородный газ может стать важной альтернативой.
Кроме того, уже существуют методы производства бензина, в которых используется процесс электролиза воды. Посмотрите, как это сделано в тексте Ученые смогли превратить углекислый газ в бензин.
Дженнифер Фогача
Учитель химии
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/eletrolise-agua.htm


