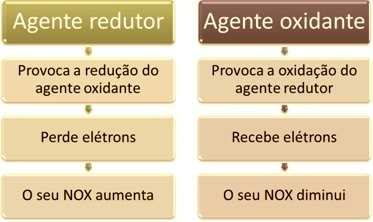
Одна из основных особенностей, отличающих окислительно-восстановительную реакцию (или окислительно-восстановительный потенциал) других - это присутствие окислителя и восстановителя, которые можно определить следующим образом:
Например, посмотрите на химическую реакцию ниже, когда алюминий (Al) корродирует в водном растворе соляной кислоты (HCl). Атомы алюминия переносят электроны на катионы H+(здесь) и производят катион Al3+(здесь):
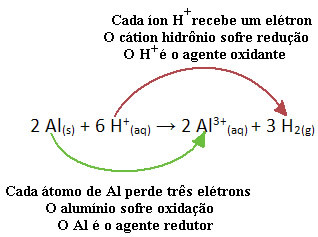
Обратите внимание: поскольку Al переносил электроны, это означает, что он вызвал сокращение катионов H+(здесь); вот почему его зовут Восстановитель. Уже катион H+(здесь) удалил электроны из алюминия, вызывая окисление из этого металла; поэтому он действует как окислитель.
В повседневной жизни существует множество примеров действия окислителей и восстановителей. Посмотрите на некоторые из них и помните, однако, что во всех случаях восстановление происходит одновременно с окислением; следовательно, если есть восстанавливающий агент, есть также окислитель.
- Примеры восстановителей:
- В фотопленках: фотопленки содержат светочувствительные соли серебра. В местах падения света происходит уменьшение количества ионов Ag.+, в результате чего наблюдается контраст, наблюдаемый на негативах.

- Витамин C: Витамин С (L-аскорбиновая кислота) - мощный восстановитель в водном растворе. Он обладает исключительной способностью окисляться, поэтому его широко используют, особенно в пищевых продуктах, в качестве антиоксидант, то есть он добавляется в другие продукты и защищает их от возможного окисления за счет собственного жертва. Примером могут служить такие фрукты, как яблоки и груши, которые темнеют при контакте с кислородом воздуха из-за окисления. Но когда вы добавляете к фруктам небольшое количество апельсинового или лимонного сока (которые содержат витамин С) разрезать, это предотвращает возникновение этой реакции, потому что витамин С действует как восстановитель и окисляется раньше, чем плод.

- Водородный газ: газообразный водород (H2) используется в ракетных двигателях и считается одной из наиболее важных альтернативных источников энергии, поскольку при его сгорании выделяется большое количество энергии и не загрязняются вещества. В этой реакции водород действует как восстановитель, окисляясь кислородом.
- Примеры окислителей:
- При производстве уксуса: при контакте с воздухом вино превращается в уксус, основным компонентом которого является уксусная кислота. Это связано с тем, что этиловый спирт или этанол, присутствующие в вине, окисляются при контакте с кислородом воздуха, в результате чего образуется уксусная кислота. Таким образом, кислород является окислителем. Даже происхождение термина «окисление» связано с реакцией с кислородом.

- В ржавчине: как указано в предыдущем примере, кислород действует как окислитель спирта; И это происходит также при контакте с различными металлами, такими как железо, вызывая процесс ржавления. Помимо кислорода воздуха, другими окислителями в данном случае являются вода или кислый раствор.
- В отбеливателях: отбеливающий эффект отбеливателей обусловлен наличием следующих двух восстановителей: o анион гипохлорита (обычно в форме натриевой соли - NaOCl), присутствующий, например, в отбеливателе; и перекись водорода (H2O2), продаваемый как перекись водорода. Эти два соединения имеют очень сильную тенденцию к окислению и вызывают восстановление других химических соединений. Следовательно, они отвечают за окисляющие вещества, придающие продуктам темный цвет. Например, в целлюлозе лигнин расщепляется и становится более легким и податливым. В случае удаления пятен и отбеливания ткани эти окислители вызывают окисление органических молекул, таких как жиры и красители.

- В алкотестерах: простой одноразовый алкотестер состоит из прозрачной трубки, содержащей водный раствор дихроматной соли калия и кремнезема, смоченный серной кислотой; смешанный с оранжевым цветом. Эта соль при контакте с парами спирта, содержащимися в дыхании пьяного водителя, вступает в реакцию, меняя цвет на зеленый. Это означает, что происходит окисление этанола (спирта) до этаналя.

Дженнифер Фогача
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm

