Если бы можно было очень четко визуализировать структуру металла, мы бы увидели его, как на изображении выше. Атомная структура металлов кристаллическая, она состоит из катионов металлов, окруженных электронами.
Кристаллические решетки, присутствующие в металлах, можно представить следующим образом: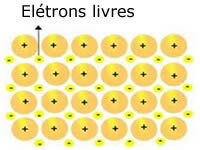
Представление металлического натрия (Na)
Кристаллические решетки металлов образованы группой закрепленных катионов.
Каждый катион Na + окружен электронами, но они делокализованы, то есть не притягиваются ни к какому ядру.
Поскольку нет притяжения между отрицательными зарядами (электроном) и положительным ядром (катионом), свободные электроны в конечном итоге занимают всю кристаллическую решетку металла. Свобода, которой обладают электроны, заставляет их образовывать электронное облако.
Способность металлов проводить электричество объясняется наличием этого облака. Электрический ток возникает в результате контакта свободных электронов с другими металлами.
В составе любого атома, включая такие металлы, как натрий (Na), золото Au, медь (Cu), присутствует валентный слой. Электроны свободно перемещаются через этот слой, поддерживая электромагнитное притяжение катионов. Это структурное свойство позволяет образовывать металлические молекулы и, следовательно, сами металлы.
Лирия Алвес
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/como-se-forma-ligacao-metalica.htm