В межмолекулярные силы они представляют собой силы электростатического притяжения, функция которых заключается в объединении молекул (молекулярных соединений), поддержании их в твердом или жидком состоянии. Они чрезвычайно важны, так как определяют все физические свойства (точка плавления, точка кипения, плотность и растворимость) веществ.
В этом тексте мы изучим взаимосвязь межмолекулярных сил и температуры кипения веществ. Для начала вспомним три важных типа межмолекулярных сил, а именно:
♦ диполь диполь: сила, возникающая в полярных молекулах. Поскольку эти молекулы имеют положительный и отрицательный полюсы, диполь-дипольная сила основана на притяжении между положительным концом одной молекулы и отрицательным концом другой. Примеры: HCl, HBr, SO.2 и PH3
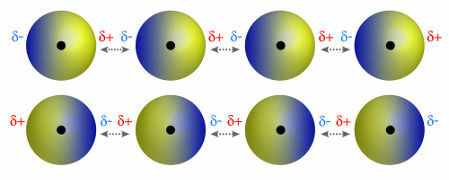
Молекулы с положительным и отрицательным полюсами притягивают друг друга.
♦ Индуцированный диполь: межмолекулярная сила, которая возникает только в неполярных молекулах (у них нет полюсов). При сближении двух неполярных молекул происходит мгновенная деформация их облаков. электронов, что вызывает дисбаланс в электронах молекулы, которые распределены в по-другому для нее. В этот момент создается кратковременный диполь, и у молекулы на мгновение появляется положительный и отрицательный полюсы, которые вызывают притяжение. Примеры: CO
2, CH4 и BH3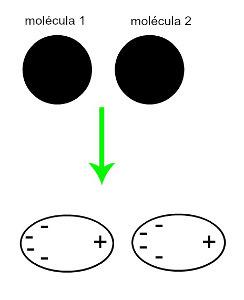
Приближение двух неполярных молекул порождает деформацию и, как следствие, перераспределение электронов, которое образует мгновенные диполи
♦ Водородные связи: это межмолекулярная сила, которая возникает в полярных молекулах, но только в тех, в которых атомы водорода обязательно связаны непосредственно с атомами фтора, кислорода или азота. Его можно рассматривать как диполь-дипольную силу, но гораздо большей интенсивности. Взаимодействие всегда происходит между водородом одной молекулы и другим атомом (F, O, N) другой молекулы. Примеры: H2O, NH3 и ВЧ
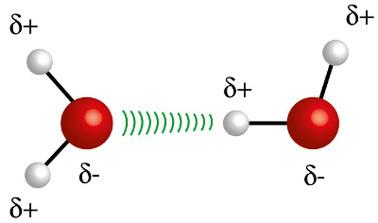
Атом водорода (белая сфера) одной молекулы взаимодействует с кислородом (красная сфера) другой молекулы воды.
Вспомнив о трех межмолекулярных силах, мы можем теперь связать их с температурой кипения веществ. называется точка кипения температура, при которой молекулы данного вещества перестают находиться в жидком состоянии (нарушаются их межмолекулярные силы) и переходят в газообразное состояние. Интересная деталь заключается в том, что межмолекулярные силы и температура кипения веществ имеют очень интенсивную и прямую взаимосвязь, поскольку чем интенсивнее межмолекулярная сила, тем выше температура кипения. Порядок интенсивности межмолекулярных сил:
Индуцированный диполь
Таким образом, мы можем сделать вывод, что молекулы с водородными связями в качестве силы взаимодействия имеют более высокие температуры кипения, чем молекулы с диполь-дипольными связями и так далее. В таблице ниже показаны три вещества и их значения температуры кипения:
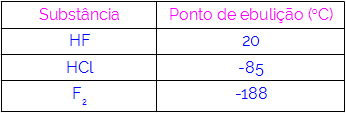
В таблице мы видим, что HF имеет более высокую температуру кипения, так как его молекулы соединены водородными связями. Вещество F2 у него самая низкая температура кипения, так как его молекулы притягиваются индуцированным диполем.
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/forcas-intermoleculares-ponto-ebulicao-das-substancias.htm
