О титан — химический элемент с символом Ti и атомным номером, то есть числом протонов, равным 22. Этот металл находится в 4 и 4 группе периодической таблицы.
Атомная масса элемента составляет 47,867 ед., и поскольку он имеет 22 электрона в электронах атома, его электронное распределение равно 1s.2 2 с2 2р6 3 с2 3р6 4 с2 3д2.
Титан обладает желательными свойствами для множества применений, поскольку он такой же прочный, как сталь, и намного легче.
Поскольку это пластичный, тугоплавкий, устойчивый к коррозии металл, он обладает механической стойкостью, термическая стабильность и низкая реакционная способность, его добавляют в металлические сплавы, чтобы они обладали высокой производительность. Его биосовместимость и нетоксичность также делают его пригодным для изготовления костных протезов.
Основные характеристики титана:
- Температура плавления: 1668°С
- Температура кипения: 3287°С
- Плотность: 4,5 г/см3
- Цвет: серебристо-серый
- Физическое состояние при 20 °C: твердое
- Изотопы: Ti46, ты47, ты48, ты49 а вы50
Этот химический элемент был открыт англичанином Уильямом Грегором в 1791 году, а его название произошло от греческого титаны, позже приписанный Мартином Генрихом Клапротом.
Титан является девятым по распространенности элементом на планете и содержится в земной коре в таких рудах, как рутил (TiO2) и ильменит (FeTiO3). Поэтому добыча полезных ископаемых является основным способом получения этого металла.
Для чего используется титан?
Поскольку он химически неактивен при комнатной температуре, легко формуется, обладает высокой механической и коррозионной стойкостью, титан используется в качестве стратегического металла.
Авиационная и аэрокосмическая промышленность являются основными потребителями титана для производства деталей, таких как компоненты турбины и фюзеляжа. Другими областями применения являются производство зубных протезов, хирургических имплантатов и ювелирных изделий.
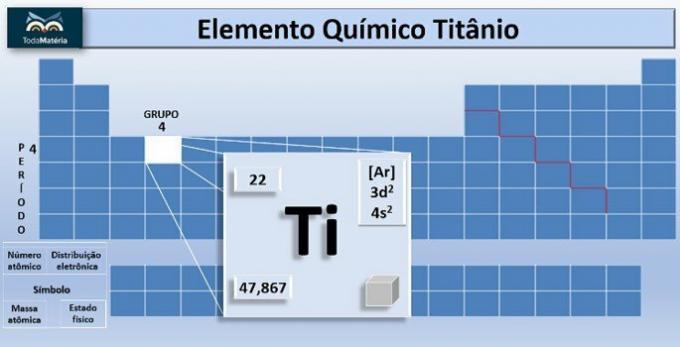
В медицине титан очень полезен из-за его совместимости с тканями человека, легкости и прочности. Он используется для производства имплантатов для частей тела, таких как фиксирующие винты, замена коленного сустава, протезы плечевой кости, протезы бедра и другие.
Диоксид титана (TiO2) является одним из основных соединений этого элемента, используемым в качестве отбеливателя. Как правило, высококачественные белые чернила используют его для улучшения внешнего вида цвета и блеска. Другие продукты, такие как зубные пасты и солнцезащитные кремы, также используют пигмент. Существует также применение в качестве пищевого красителя, добавляемого в молочные продукты, сладости и напитки.
В архитектуре мы можем увидеть использование титана для покрытия изогнутых конструкций в Музее Гуггенхайма в Бильбао, северная Испания.

В повседневной жизни мы можем встретить множество продуктов, в состав которых входит титан, например, велосипедные рамы, очки и теннисные ракетки.
В химической промышленности титан используется в качестве катализатора реакций. Таким образом, можно регулировать скорость реакции и сокращать время образования продукта, не влияя на состав веществ.
Автомобильная промышленность изучала использование титана при производстве автомобилей для уменьшения их массы и, таким образом, снижения расхода топлива и увеличения их ускорения.
Получите больше знаний с содержанием:
- Химические элементы
- Периодическая таблица
- Что такое металлы?
Библиографические ссылки
АТКИНС, П. В.; ДЖОНС, Л. Принципы химии: вопросы современной жизни и окружающей среды. 3 изд. Порту-Алегри: Книжник, 2006.
ФЕЛЬТРЕ, Р. Основы химии: т. 1, с. не замужем. 4-е изд. Сан-Паулу: Модерна, 2005.
Ли, Дж. Д. Не такая краткая неорганическая химия. Перевод 5-го изд. Английский. Издательство Эдгард Блюхер Лтд. 1999.