НАШИ периодическая классификация элементов был предложен в 1913 году Генри Монсли (1887-1915), который определил периодическое изменение многих свойства через равные промежутки времени в зависимости от числа протонов в ядре атома элемента хим.
Из-за Закон периодичности, критерием, используемым для организации элементов текущей Периодической таблицы, является порядок возрастания атомного номера (Z).
118 химических элементов расположены в группах и периодах периодической таблицы. По физико-химическим свойствам различают металлы, неметаллы (неметаллы) и полуметаллы (металлоиды).

Вертикальные линии – это 18 групп таблицу и сопоставьте элементы со схожими химическими свойствами. Горизонтальные линии соответствуют 7 периодов и представляет элементы с одинаковым количеством электронных слоев.
Водород — это элемент, который стоит выше группы 1 из-за своего электронного распределения, но не имеет с ними общих характеристик.
Проверьте Периодическая таблица полный и обновленный.
металлы
Большинство химических элементов периодической таблицы относятся к металлам. К основным характеристикам металлов относятся:
- Имеют характерный блеск;
- Они плотные, податливые и пластичные;
- Они являются хорошими проводниками электричества и тепла;
- Они присутствуют в условиях окружающей среды в твердом состоянии, за исключением ртути.
Металлические элементы периодической таблицы:
щелочные металлы (группа 1): литий, натрий, калий, рубидий, цезий и франций.
щелочноземельные металлы (группа 2): бериллий, магний, кальций, стронций, барий и радий.
Представительские вопросы, кроме элементов 1 и 2 группы, являются: алюминий, галлий, индий, таллий, нион, олово, свинец, флеровий, висмут, мусковий и ливерморий.
Внешние переходные металлы Элементы, занимающие центральную часть Периодической таблицы:
- Группа 3: скандий и иттрий.
- Группа 4: титан, цирконий, гафний и резерфордий.
- Группа 5: ванадий, ниобий, тантал и дубний.
- Группа 6: хром, молибден, вольфрам и сиборгий.
- Группа 7: марганец, технеций, рений и борий.
- Группа 8: железо, рутений, осмий и гассий.
- Группа 9: кобальт, родий, иридий и мейтнерий.
- Группа 10: никель, палладий, платина, дармстадий.
- Группа 11: медь, серебро, золото и рентген.
- Группа 12: цинк, кадмий, ртуть и коперниций.
Внутренние переходные металлы - элементы, входящие в группу 3 и соответствующие элементам ряда лантанидов и актиноидов.
Ряд лантаноидов состоит из лантана, церия, празеодима, неодима, прометия, самария, европия, гадолиния, тербия, диспрозия, гольмия, эрбия, тулия, иттербия и лютеция.
Ряд актинидов содержит элементы актиний, торий, протактиний, уран, нептуний, плутоний, америций, кюрий, берклий, калифорний, эйнштейний, фермий, менделевий, нобелий и лоренс.
Узнайте больше о щелочные металлы.
неметаллы
Неметаллы расположены в правой части Периодической таблицы и имеют противоположные металлам характеристики, например:
- Они не имеют блестящего вида;
- Они плохо проводят электричество и тепло, поэтому их используют как изоляторы;
- У них низкие температуры кипения и плавления, поэтому многие из них встречаются в природе в жидком состоянии.
Ты неметаллические элементы Периодической таблицы: водород, азот, кислород, углерод, фосфор, селен, сера, галогены и инертные газы.
Ты галогены Это элементы, принадлежащие к группе 17: фтор, хлор, бром, йод, астат, тенессин и семейство инертных газов.
Ты благородные газы относятся элементы, относящиеся к 18 группе: гелий, неон, аргон, криптон, ксенон, радон, оганессон.
Узнайте больше о благородные газы и галогены.
полуметаллы
Полуметаллы или металлоиды: бор, кремний, германий, мышьяк, сурьма, теллур и полоний. Эти элементы имеют промежуточные характеристики между металлами и неметаллами.
Также читайте о семейства периодических таблиц.
Репрезентативные и переходные элементы
Другой способ классификации элементов состоит в разделении их на репрезентативные и переходные элементы в соответствии с электронное распределение атома.
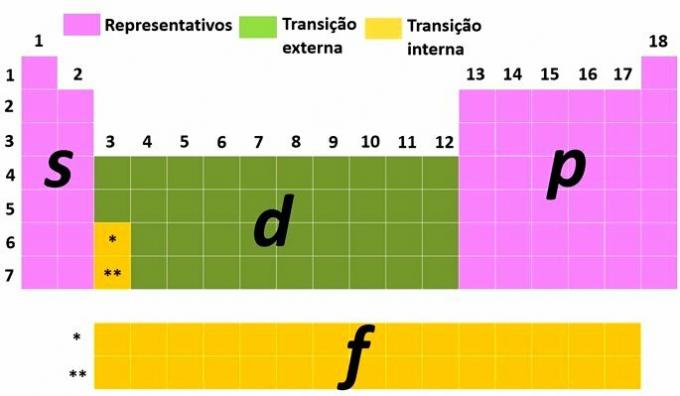
Ты репрезентативные элементы те, у которых электронная конфигурация заканчивается самым энергетическим подуровнем в с (группы 1 и 2) или для (группы 13, 14, 15, 16, 17 и 18).

Ты переходные элементы разделены на внешний переход, с элементами, которые имеют самый энергичный электрон на подуровне г и те из внутренний переход, где самый энергичный электрон находится на подуровне ф.

Получите больше знаний с содержанием:
- периодические свойства
- Упражнения с периодической таблицей
- Упражнения по организации периодической таблицы


