В реакции горения они присутствуют во многих аспектах нашей повседневной жизни. Например, основные источники выработки энергии возникают в результате сжигания определенных видов топлива, таких как этанол, бензин, древесный уголь и другие. Кроме того, энергия, необходимая нам для выживания и выполнения работы, является результатом реакций горения, которые происходят внутри наших клеток, когда мы «сжигаем» пищу, которую едим.
Но что нужно для реакции горения?
Необходимы три вещи:
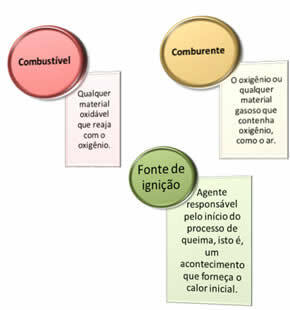
Эти три фактора составляют огненный треугольник, потому что, как только начинается реакция горения, высвобождаемая энергия поддерживает реакцию и позволяет ей продолжаться до тех пор, пока не исчезнут топливо, окислитель или тепло (выделенная энергия). Это означает, что будет Цепная реакция.
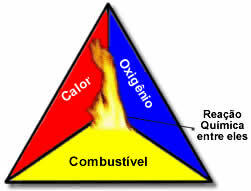
Например, если кто-то бросит в лесу зажженную сигарету, произойдет пожар (реакция горения). В этом случае куст это топливо, O кислород присутствует в воздухе атмосферный окислитель это сигарета горит был источник возгорания. Это горение будет продолжаться до тех пор, пока не будет устранен один из трех факторов. Если пожарные бросят воду, жар исчезнет. Но даже если ничего не предпринять, чтобы остановить это горение, в какой-то момент оно прекратится, то есть когда закончится топливо (лес).
Как уже упоминалось, в этих реакциях выделяется тепло, поэтому горение является экзотермической реакцией. Однако это реакция неполного сгорания. Чтобы понять почему, посмотрите разницу между полным и неполным сгоранием:
Полное сгорание:
Анализируя органические соединения в качестве топлива, мы должны:
| В полное сгорание это произойдет, когда углеродная цепь разорвана и все атомы углерода в углеродной цепи полностью окислены. |
| Ты формованные изделия по углеводородам будет CO2 (углекислый газ) и ЧАС2О (Воды). |
Наблюдайте за полным сгоранием изооктана, который является одним из компонентов бензина.
Ç8ЧАС18 (г) +25/2 O2 (г) → 8 СО2 (г) + 9 часов2О(1)
неполное сгорание
| В этом случае не хватает окислителя, то есть кислорода, чтобы сжечь все топливо. |
| Таким образом, образующиеся продукты CO (окись углерода) и ЧАС2О. |
Обратите внимание на то же горение изоктана, но теперь не полностью:
Ç8ЧАС18 (г) + 17/2 O2(грамм) → 8 СО (грамм) + 9 часов2О(1)
Примером может служить сжигание лесов, так как полученные выбросы состоят из CO и определенных веществ, таких как сажа (C), а также золы и других простых и сложных органических соединений. Оксид азота, озон и альдегиды также могут образовываться в результате вторичных реакций из-за присутствия в воздухе других компонентов.
Ç8ЧАС18 (г) + 9/2 O2 (г) → 8С (грамм) + 9 часов2О(1)
Дженнифер Фогача
Окончила химический факультет
Бразильская школьная команда
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm