Атомные модели возникли из-за необходимости объяснять структуру атомов. Когда были представлены новые доказательства строения атомов, новая атомная модель попыталась прояснить эти открытия.
Греческие философы Демокрит и Левчипо в V веке; Ç. называется атом, от греческого ατoμoν, неделимая частица и мельчайшая часть материи.
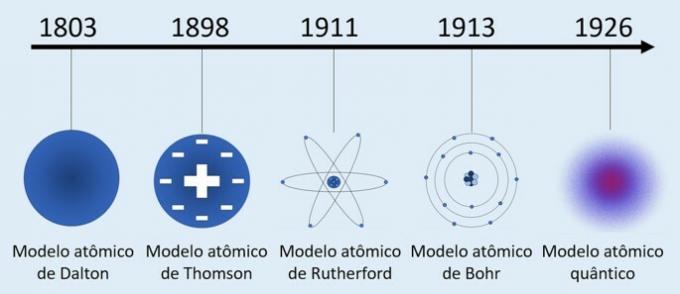
Хотя концепция атома устарела, развитие атомных теорий восходит к 19 и 20 векам. Поэтому основные атомные модели, разработанные для понимания природы материи, были:
- Модель атома Далтона (1803 г.) - «Модель бильярдного шара»
- Модель атома Томсона (1898 г.) - "Модель дождевого пудинга"
- Атомная модель Резерфорда (1911) - «Ядерная модель»
- Атомная модель Бора (1913 г.) - «Планетарная модель»
- Квантовая модель атома (1926 г.) - «Модель электронного облака».
Атомная модель Дальтона
Первая признанная попытка описания атомов была предпринята английским ученым Джоном Далтоном (1766-1844) в модели, которая стала широко известной как «бильярдный шар».
Атом Далтона (1803): массивная, неделимая и неразрушимая сфера.

По словам Далтона:
- Все вещества состоят из атомов;
- Атомы химического элемента идентичны по размеру и характеристикам, тогда как атомы разных химических элементов различны;
- Вещества являются результатом химической реакции, состоящей из рекомбинации атомов.
Отрицательные моменты: поскольку электроны еще не были известны, когда Дальтон сформулировал свою теорию, эти частицы, которые, как мы теперь знаем, являются частью атомов, не рассматривались.
Узнать больше о Атомная модель Дальтона.
Модель атома Томсона
Джозеф Джон Томсон (1856-1940) был ответственен за открытие существования электронов, частиц, наделенных отрицательным зарядом, которые являются частью атомов. Это открытие опровергло атомную теорию Дальтона, согласно которой атом неделим, но образован еще более мелкими частицами, и поэтому он стал известен как «пудинг с изюмом».
Атом Томсона (1898): положительно заряженная сфера с неподвижными электронами.

По словам Томсона:
- Атом электрически нейтрален;
- Электроны прикрепляются к положительно заряженной поверхности;
- Между электронами, распределенными по атомам, возникает отталкивание.
Отрицательные моменты: Хотя Томсон принял во внимание существование электронов, атом не является положительной сферой, а скорее наделен положительно заряженные частицы, протоны, идентифицированные в 1886 году ученым Юджином Гольдштейном и позже подтвержденные Эрнестом Резерфорд.
Узнать больше о Атомная модель Томсона.
Атомная модель Резерфорда
В ходе своих экспериментов Эрнесту Резерфорду (1871-1937) удалось продемонстрировать, что атом не является неделимой частицей, как считалось, а состоит из более мелких частиц.
Атом Резерфорда (1911): положительно заряженное ядро и электроны расположены вокруг него в электросфере.
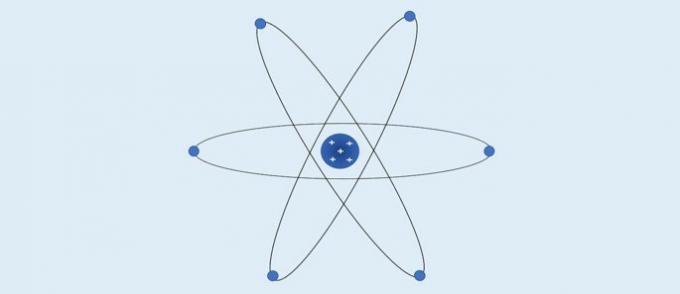
По словам Резерфорда:
- Атом имеет центральную область с высокой концентрацией положительного заряда;
- Масса атома сосредоточена в его центральной области;
- Электроны легче и расположены вокруг ядра - области, содержащей много пустых пространств.
Отрицательные моменты: в атомном ядре есть не только положительно заряженные частицы, но и другие субатомные частицы, нейтроны, открытые Джеймсом Чедвиком в 1932 году. Более того, модель, предложенная Резерфордом, не объясняла излучение света атомами.
Узнать больше о Атомная модель Резерфорда.
Атомная модель Бора
Стремясь объяснить, почему элементы излучают характерные цвета при воздействии определенных условий и в зависимости от Модель атома Резерфорда, Нильс Бор (1885-1962) предложил атомную теорию, которая объяснила излучение света в определенных частоты.
Атом Бора (1913): электроны движутся фиксированными круговыми слоями вокруг ядра.
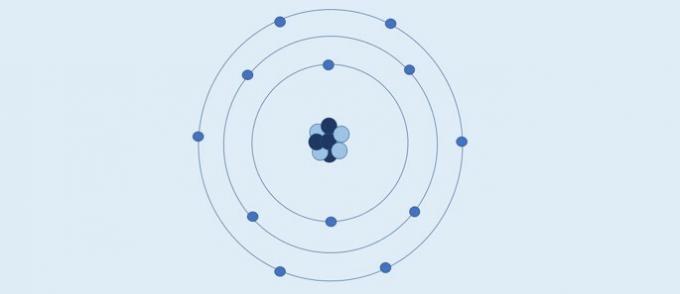
По словам Бора:
- Электроны движутся слоями вокруг ядра;
- Слои вокруг ядра имеют определенные значения энергии;
- Чтобы перейти на более внешний уровень, электрон должен поглотить энергию. Вернувшись в слой ближе к ядру, электрон выделяет энергию.
Отрицательные моменты: нельзя сказать, что электроны перемещаются вокруг ядра в фиксированных положениях, как планеты вокруг Солнца.
Узнать больше о Атомная модель Бора.
Квантовая модель атома
Многие ученые внесли свой вклад в развитие квантовой механики, которая пытается объяснить «более реальную» структуру атом сочетанием нескольких исследований и, следовательно, является наиболее сложным.
Квантовый атом (1926): ядро состоит из протонов (положительный заряд) и нейтронов (нулевой заряд), а электроны (отрицательный заряд) образуют электронное облако вокруг ядра.
Согласно квантовой модели атома:
- Ядро состоит из протонов и нейтронов. Поскольку зарядом обладают только протоны, ядро заряжено положительно;
- Электроны образуют электронное облако вокруг ядра;
- Электроны движутся по орбиталям в трехмерном пространстве;
- Точное положение электрона определить невозможно. Что делается, так это вычисления, которые определяют вероятность того, что электрон будет находиться в данной области в данный момент времени.
Ты квантовые числа имеют функцию определения местоположения электронов. Они:
О главное квантовое число (n) представляет собой энергетические уровни, то есть электронные слои атома.
О вторичное квантовое число (l) указывает энергетические подуровни, то есть энергетический подуровень, которому принадлежит электрон.
О магнитное квантовое число (m) обозначает орбиту, на которой встречаются электроны.
Узнать больше о атомные модели и проверь свои знания с упражнения на атомных моделях.