В реакции гидратации в алкадиены они есть реакции присоединения, то есть компоненты (гидроксоний и гидроксид) молекулы воды добавляются к алкадиену.
Ты алкадиены представляют собой углеводороды, которые имеют открытую цепь и две двойные связи (образованные сигмой и пи) между атомами углерода, как мы можем видеть в следующей структуре:

Структурная формула алкадиена
для реакция гидратации в алкадиенах необходимо, чтобы пи-связь, присутствующая в двойной связи, была разорвана под действием тепла и серной кислоты (H2ТОЛЬКО4). При разрыве пи-связи появляются два сайта связывания, каждый на одном из атомов углерода, участвующих в двойной связи.

Появление сайтов связывания с нарушением связывания пи
Появление центров связывания на молекуле алкадиена необходимо для ионов (H+ и ох-) из воды добавляются к алкадиену, образуя, например, диалкогольный спирт (алкоголь с двумя гидроксилами).
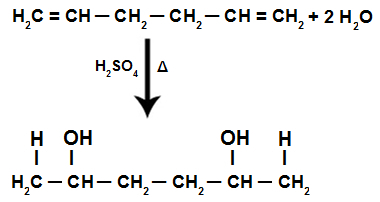
Добавление H+ и ох- в структуре алкадиена
ПРИМЕЧАНИЕ: Добавление H+ и ох- в структуре алкадиена следует Правило марковникова
, т.е. H+ связывается с наиболее гидрогенизированным углеродом, а ОН- связывается с менее гидрогенизированным углеродом.
Пример применения правила Марковникова при гидратации алкадиенов
Поскольку существуют разные типы алкадиенов в зависимости от положения двойных связей, возможно, что при гидратации алкадиена образуются разные соединения. См. Следующие случаи:
→ Накопленный или конденсированный алкадиен
Это алкадиен, который имеет две двойные связи, одновременно включающие три атома углерода, то есть нет одинарной связи, разделяющей атомы углерода, участвующие в связях удваивается.

Структурная формула накопленного алкадиена
Во время реакции гидратации чередующегося алкадиена пи-связи разрываются, H+ добавлен к более гидрогенизированным углеродам и ОН- добавлено к менее гидрогенизированным углям:
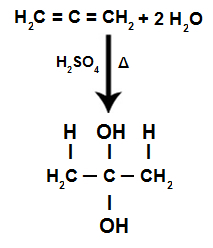
Уравнение реакции накопленной гидратации алкадиена
Мы видим, что при гидратации накопленного алкадиена один и тот же атом углерода получает два гидроксила, образуя двойной спирт, который представляет собой нестабильную структуру.

Состав образовавшегося двойного диаспирта
Поскольку двойной спирт нестабилен, мы имеем образование молекулы воды с компонентами двух гидроксилов и создание пи-связи между углеродом и кислородом.

Образование кетона из двойного спирта
Следовательно, реакция гидратации накопленных алкадиенов приведет к образованию кетон.
→ Конъюгированный или альтернативный алкадиен
Это алкадиен, который имеет две двойные связи, одновременно включающие четыре атомы углерода, то есть существует одинарная связь, разделяющая атомы углерода, участвующие в связях удваивается.
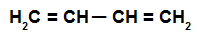
Структурная формула чередующегося алкадиена
В чередующихся алкадиенах возникает резонанс их двойных связей. Таким образом, электроны пи-связи меняют положение (красные стрелки), как на следующей диаграмме:
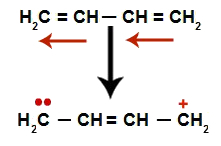
Схема, изображающая резонанс в чередующемся алкадиене
В общем, мы имеем появление двойной связи точно между атомами углерода там, где раньше были два двойных атома, и создание двух участков связывания, по одному на каждом атоме углерода, который больше не образует двойную связь (в примере, атомы углерода 1 и 4). Углероды 1 и 4 цепи получают H+ и ох- из воды.

Частичная гидратация в чередующемся алкадиене
После резонанса пи-связь новой двойной связи разрывается, и H+ и ох- добавляются к молекуле алкадиена. ОН добавляется к углероду, ближайшему к первой добавленной группе ОН, потому что он подвергается электронному притяжению группы, которая является более электроотрицательной.

Прекращение гидратации в чередующемся алкадиене
Из-за резонанса мы говорим, что чередующийся алкадиен претерпел 1,4 гидратации, образуя диалкоголь.
→ С изоляцией из алкадиена
Это алкадиен, который имеет две двойные связи, содержащие одновременно не менее пяти атомов. углерода, то есть есть по крайней мере две одинарные связи, разделяющие атомы углерода, входящие в эти связи. удваивается.

Структурная формула изолированного алкадиена
Во время реакции гидратации изолированного алкадиена пи-связи разрываются, образуя H+ добавлен к более гидрогенизированным углеродам и ОН- добавлен к менее гидрогенизированным углям.

Уравнение реакции гидратации изолированного алкадиена
Следовательно, при добавлении изолированного алкадиена образуется только диалкоголь.
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm