Точка плавления и точка кипения представляют собой температуру, при которой вещество меняет состояние при заданном давлении.
В случае точки плавления вещество переходит из твердого состояния в жидкое. Точка кипения относится к переходу из жидкого состояния в газообразное.
Например, лед начинает превращаться в воду в жидком виде, когда его температура равна 0 ° C. Следовательно, температура плавления воды составляет 0 ° C (при давлении 1 атмосфера).
Чтобы перейти от жидкости к пару, вода должна достичь температуры 100 ° C. Таким образом, температура кипения воды составляет 100 ° C (при давлении 1 атмосфера).

Точка слияния
Когда вещество в твердом состоянии получает нагревать, увеличивается степень перемешивания его молекул. Следовательно, его температура также повышается.
При достижении определенной температуры (точки плавления) молекулы волнуются так, что они разрывают внутренние связи между атомами и молекулами.
В этот момент вещество начинает менять свое состояние и переходит в жидкое состояние, если продолжает получать тепло.
В течение Слияние его температура остается постоянной, так как полученное тепло используется исключительно для изменения состояния.

Количество тепла на единицу массы, необходимое для смены фаз, называется скрытая теплота плавления (Lж) и является характеристикой вещества.
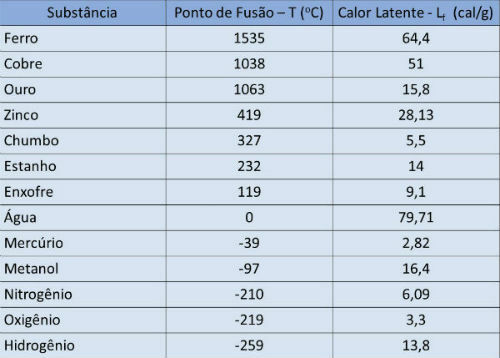
Таблица температуры плавления и скрытой теплоты
В таблице ниже мы указываем температуру плавления и скрытую теплоту некоторых веществ до атмосферное давление.
Точка кипения
THE кипячение он характеризуется быстрым переходом из жидкого в газообразное состояние с образованием паров (пузырьков) внутри жидкости.
Как и в случае плавления, существует температура (точка кипения), при которой данное вещество переходит из жидкого в газообразное состояние.
Чтобы это произошло, вещество должно получить тепло. В течение всего фазового перехода температура остается постоянной.
скрытое тепло испарение (Lv) - количество тепла на единицу массы, необходимое веществу для перехода в фазу.
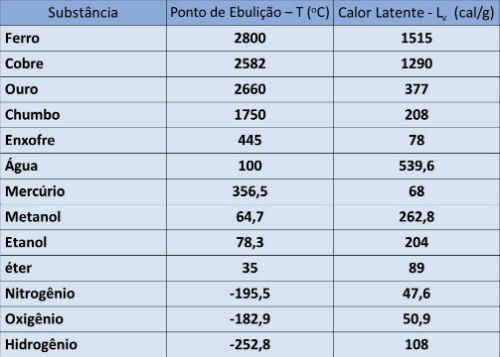
Таблица температур кипения и скрытой теплоты
В таблице ниже мы указываем температуру кипения и скрытую теплоту испарения некоторых веществ при атмосферном давлении.
Вмешательство давления
Температура точки плавления и точки кипения зависит от давления, оказываемого на вещество.
Как правило, при плавлении вещества увеличиваются в объеме. Это означает, что чем выше давление, тем выше температура, при которой вещество меняет свою фазу.
Исключение составляют некоторые вещества, в том числе вода, которая при таянии уменьшает свой объем. В этом случае более высокое давление снизит температуру плавления.

Снижение давления приводит к понижению температуры кипения данного вещества, что означает, что вещество будет кипеть при более низкой температуре.
Например, в местах над уровнем моря вода закипает при температуре ниже 100 ° C. В результате в этих местах готовят гораздо дольше, чем в местах на уровне моря.
Читайте тоже:
- Изменения физического состояния
- Термометрические весы
- Термометрические весы - упражнения
- Физические состояния воды
- Диаграмма фаз
- Затвердевание
- Конденсация
- Коллигативные свойства
- Периодические свойства
- Испарение
- Упражнения с периодической таблицей