Распределение электронов или электронная конфигурация - это способ упорядочения химических элементов с учетом количества электронов, которые они имеют, и их близости к ядру атома.
Электронное многоуровневое распределение
После появления нескольких атомных моделей модель Бора предложила организовать электросферу по орбитам.
Электроны организованы и распределены через электронные слои, некоторые из которых находятся ближе к ядру, а другие - дальше.
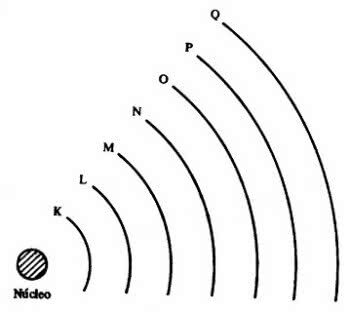
Затем появились 7 электронных слоев (K, L, M, N, O, P и Q), которые представлены горизонтальными линиями с номерами от 1 до 7 в периодической таблице.
Элементы на одних и тех же линиях имеют одинаковое максимальное количество электронов и одинаковые уровни энергии.
Таким образом, можно наблюдать, что электроны находятся на энергетических уровнях и подуровнях. Итак, у каждого есть определенное количество энергии.
|
Уровень энергии |
Электронный слой |
Максимальное количество электронов |
|---|---|---|
| 1° | K | 2 |
| 2° | L | 8 |
| 3° | M | 18 |
| 4° | N | 32 |
| 5° | О | 32 |
| 6° | п | 18 |
| 7° | Q | 8 |
THE валентный слой это последний электронный слой, то есть самый внешний слой атома. В соответствии с Правило октета, атомы имеют тенденцию стабилизироваться и становиться нейтральными.
Это происходит, когда у них одинаковое количество протонов и нейтронов с восемью электронами в последней электронной оболочке.
Позже появились энергетические подуровни, представленные строчными буквами s, p, d, f. Каждый подуровень поддерживает максимальное количество электронов:
| подуровни | Максимальное количество электронов |
|---|---|
| s | 2 |
| п | 6 |
| d | 10 |
| ж | 14 |
Диаграмма Полинга
Американский химик Линус Карл Полинг (1901–1994) изучил атомные структуры и разработал схему, которая используется до сих пор.
Полинг нашел способ расположить все энергетические подуровни в порядке возрастания, используя диагональное направление. Схема стала известна как Диаграмма Полинга.
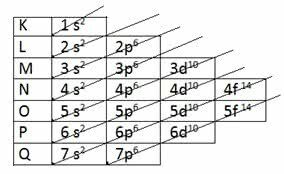
По возрастанию: 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 5 с2 4d10 5p6 6 с2 4f14 5d10 6p6 7 с2 5f14 6d10 7p6
Обратите внимание, что число, указанное перед подуровнем энергии, соответствует уровню энергии.
Например, через 1с2:
- s указывает на подуровень энергии
- 1 указывает первый уровень, расположенный на слое K
- показатель степени 2 указывает количество электронов на этом подуровне
Как сделать электронную рассылку?
Чтобы лучше понять процесс электронного распространения, посмотрите на решенное упражнение ниже.
1. Составьте электронное распределение элемента Железо (Fe) с атомным номером 26 (Z = 26):
При применении диаграммы Линуса Полинга диагонали пересекаются в направлении, указанном на модели. Энергетические подуровни заполнены максимальным количеством электронов на электронную оболочку, пока не заполнится 26 электронов элемента.
Чтобы сделать распределение, обратите внимание на общее количество электронов на каждом подуровне и в соответствующих электронных слоях:
К - с2
L - 2 с2 2p6
M - 3 с2 3p6 3d10
N - 4 с2
Обратите внимание, что не было необходимости выполнять электронное распределение во всех слоях, так как атомный номер железа равен 26.
Таким образом, электронное распределение этого элемента представляется следующим образом: 1s2 2 с2 2p6 3 с2 3p6 4 с2 3d6. Сумма чисел экспоненты составляет 26, то есть общее количество электронов, присутствующих в атоме железа.
Если электронное распределение обозначено слоями, оно представляется следующим образом: K = 2; L = 8; М = 14; N = 2.
Воспользуйтесь возможностью проверить свои знания в Упражнения по электронной дистрибуции.
В периодическая таблица, это показано следующим образом:

Читайте тоже:
- Электронное сродство
- Квантовые числа
- Упражнения с периодической таблицей
- Упражнения по организации периодической таблицы



