Объемный анализ или волюметрия это лабораторная процедура, в которой мы используем определенный объем решение в концентрация известно, чтобы определить концентрацию другого раствора. Объем раствора известной концентрации будет определен, когда он полностью прореагирует с раствором неизвестной концентрации, то есть вовлеченные растворы должны вступить в реакцию друг с другом.
Наиболее часто используемые инструменты для измерения заданного объема:
- Пипетка

Пример пипетки, используемой для измерения объема
- Бюретка

Бюретка - важное оборудование для измерения объема.
Измерение объема производится путем оценки высоты так называемого мениска., который представляет собой не что иное, как область поверхности жидкости, которая имеет прямоугольную или куполообразную форму (форму капли), в зависимости от толщины емкости. Чем шире емкость, тем прямоугольнее мениск; чем тоньше емкость, тем она будет более выпуклой. Чтобы оценить мениск, глаз должен находиться точно на его высоте, и мы должны использовать нижнюю область в качестве ориентира, если мениск прямоугольный, или кончик, если он выпуклый. См. Изображение оценки:
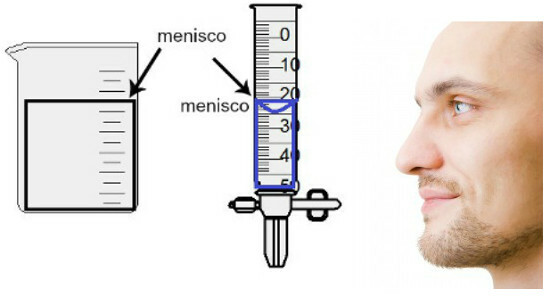
Чтобы оценить мениск, важно, чтобы ваши глаза смотрели на него.
В объемном анализе наиболее часто используемым оборудованием является бюретка. Это связано с тем, что, поскольку метод включает химические реакции, которые можно быстро обрабатывать, бюретка позволяет жидкость выходит на его кончике каплями, что позволяет нам остановить выход жидкости больше контролируется.
Одна из наиболее часто используемых процедур в волюметрии - это титрование. Это объемный анализ, который включает возникновение реакции между кислотой и основанием или наоборот. Необходимое для его реализации оборудование представлено на изображении ниже:
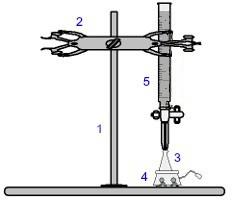
Изображение оборудования, используемого для титрования
Цифры синего цвета означают:
1) Универсальная опора;
2) Коготь (используется для удержания бюретки);
3) Эрленмейер (получает раствор неизвестной концентрации);
4) Магнитная мешалка (используется для перемешивания раствора, находящегося в колбе Эрленмейера);
5) Бюретка (принимает раствор известной концентрации).
В колбу Эрленмейера добавляют объем раствора неизвестной концентрации с индикатором фенолфталеина (раствор сразу станет розовым). В бюретку помещается определенный объем раствора известной концентрации. Затем раствор кислоты из бюретки напрямую капают в основной раствор в колбе Эрленмейера. Это капание длится до тех пор, пока основной раствор не станет бесцветным, и в этот момент мы называем точку поворота, которая указывает, что все основание, присутствующее в растворе, полностью прореагировало с кислотой.
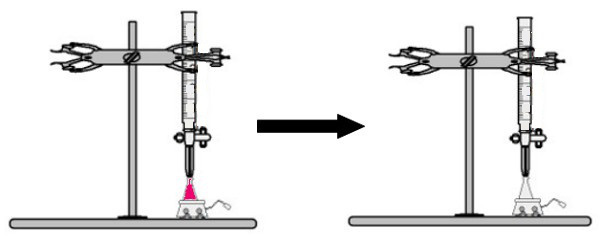
В переломный момент раствор перестает быть розовым и становится бесцветным.
Наблюдение: Если раствор неизвестной концентрации является кислотным, то при получении индикатора фенолфталеина он будет бесцветным. Таким образом, поворотный момент в титровании наступит, когда кислотный раствор станет розовым при получении основного раствора из бюретки.
Наконец, чтобы определить концентрацию основного раствора, просто используйте следующее уравнение:
Ma.Va = Mb.Vb
Ma = молярность кислоты;
Va = объем кислоты;
Mb = молярность основания;
Vb = базовый объем.
Теперь рассмотрим пример того, как выполняется расчет раствора с неизвестной молярностью.
1) 30 мл раствора неизвестного основания добавляли в колбу Эрленмейера, чтобы выполнить титрование для определения его концентрации (молярности). В бюретку добавили 50 мл раствора кислоты с концентрацией 0,2 моль / л. После добавления кислотного раствора по каплям и до тех пор, пока основной раствор не был титрован, было замечено, что для титрования использовалось 20 мл кислотного раствора. Определите молярность используемого основного раствора.
Данные об упражнениях:
Vb = 30 мл
Mb =?
Ma = 0,2 моль / л
Va = 20 мл
Поскольку молярность кислоты и ее объем составляют соответственно 0,2 моль / л и 20 мл, а объем используемого основания составляет 30 мл, просто используйте формулу титрования:
Ma.Va = Mb.Vb
0.2.20 = Мб.30
4 = Мб.30
4 = МБ
30
Mb = 0,133 моль / л
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/analise-volumetrica.htm

