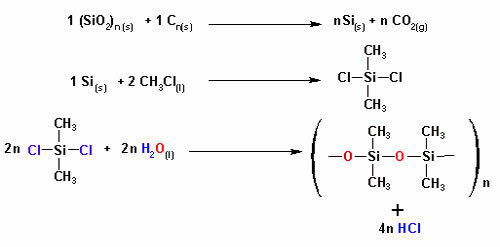
Ниобий (Nb) - химический элемент с атомным номером 41, принадлежащий к группе 5 периодической таблицы.
Это естественно доступный переходный металл в твердом состоянии, который был открыт в 1801 году британским химиком Чарльзом Хэтчеттом.
Минералы, содержащие ниобий, редки в мире, но изобилуют в Бразилии, стране с самыми большими запасами этого металла.
Благодаря своим свойствам, высокой проводимости и коррозионной стойкости этот элемент находит множество применений, от производства стали до производства ракет.
Далее мы познакомим вас с этим химическим элементом и характеристиками, которые делают его таким важным.
Что такое ниобий?
Ниобий - тугоплавкий металл, то есть очень устойчив к нагреванию и износу.
Металлы этого класса: ниобий, вольфрам, молибден, тантал и рений, причем ниобий является самым легким из всех.
Ниобий встречается в природе в виде минералов, обычно связанных с другими элементами, в основном с танталом, поскольку они имеют очень похожие физико-химические свойства.
Этот химический элемент классифицируется как переходный металл в периодической таблице. Он яркий, малой твердости, с низким сопротивлением прохождению электрического тока и устойчив к коррозии.
Физические свойства ниобия
| физическое состояние | твердый при комнатной температуре |
|---|---|
| цвет и внешний вид | металлический серый |
| Плотность | 8,570 г / см3 |
| Точка слияния | 2468 ° С |
| Точка кипения | 4742 ° С |
| Кристаллическая структура | Тело центрированный кубик - CCC |
теплопроводность |
54,2 Вт м-1 K-1 |
Химические свойства ниобия
| Классификация | переходный металл |
|---|---|
| атомный номер | 41 |
| Блокировать | d |
| Группа | 5 |
| Курс времени | 5 |
| атомный вес | 92,90638 u |
| атомный луч | 1,429 Å |
| обычные ионы | Nb5+ и Nb3+ |
| электроотрицательность | 1.6 Полинг |
Основное преимущество использования этого металла заключается в том, что только количество этого элемента в граммах может модифицировать тонну железа, сделав металл легче, устойчивым к коррозии и многому другому эффективный.
Где находится ниобий?
По сравнению с другими веществами, присутствующими в природе, ниобий имеет низкую концентрацию - 24 части на миллион.
Этот металл встречается в следующих странах: Бразилия, Канада, Австралия, Египет, Демократическая Республика Конго, Гренландия, Россия, Финляндия, Габон и Танзания.
Ниобий в Бразилии
В 1950-х годах бразильский геолог Джалма Гимарайнш открыл в Бразилии крупнейшее месторождение пирохлорной руды, содержащей этот металл.
Большое количество руд, содержащих ниобий, находится в Бразилии, крупнейшем в мире производителе, на долю которого приходится более 90% запасов этого металла.
Разведанные запасы находятся в штатах Минас-Жерайс, Амазонас, Гояс и Рондония.
ниобиевые руды
Ниобий в природе всегда связан с другими химическими элементами. Уже известно более 90 видов минералов, содержащих ниобий и тантал в природе.
В таблице ниже мы можем увидеть некоторые из руд, которые содержат ниобий, основные характеристики и содержание ниобия, доступное в каждом материале.
| колумбит танталит | |
|---|---|
 | |
| Состав: | (Fe, Mn) (Nb, Ta)2O6 |
| Содержание ниобия (максимальное): | 76% Nb2O5 |
| Функции: |
|
| Пирохлорит | |
|---|---|
 | |
| Состав: | (В2,Здесь)2(Nb, Ti) (O, F)7 |
| Содержание ниобия (максимальное): | 71% Nb2O5 |
| Функции: |
|
| Лопарит | |
|---|---|
 | |
| Состав: | (C, Na, C)2(Ti, Nb)2O6 |
| Содержание ниобия (максимальное): | 20% Nb2O5 |
| Функции: |
|
разведка ниобия
Ниобиевые руды претерпевают преобразования до тех пор, пока не образуются продукты, которые будут продаваться.
Шаги этого процесса можно резюмировать следующим образом:
- Добыча
- Концентрация ниобия
- Очистка ниобия
- Ниобиевые продукты
Добыча ведется там, где есть запасы руды, которые извлекаются с помощью взрывчатых веществ и транспортируются лентами к месту, где происходит стадия обогащения.
Концентрация происходит при разложении руды, измельчение приводит к тому, что кристаллы руды становятся намного мельче и используются магнитная сепарация железные фракции удаляются из руды.
При очистке ниобия происходит удаление серы, воды, фосфора и свинца.
Одним из продуктов, содержащих ниобий, является сплав железа с ниобием, который производится по следующему уравнению:
Этот процесс называется алюминотермией, при котором рудный концентрат смешивается в реакторах с железным ломом или оксидом железа.
Оксиды металлов реагируют с алюминием при высоких температурах, образуя интересующий продукт.
Наиболее продаваемые продукты ниобия:
- Концентраты ниобия: основа, содержащая 58% Nb2O5.
- Сплав железо-ниобий: содержит 65% ниобия.
- Оксид высокой чистоты: используется в производстве специальных материалов.
Для чего нужен ниобий?
Характеристики ниобия делают этот элемент все более востребованным и находящим бесчисленное множество применений.
С момента его открытия в 1905 году области применения ниобия начали изучаться, когда немецкий химик Вернер фон Болтон произвел элемент в чистом виде.
50-е годы представляли собой большой поиск приложений ниобия, так как до этого он не производился в больших масштабах.
В этот период «холодная война» вызвала интерес к этому металлу для использования в аэрокосмических компонентах.
Ниже приведен список способов использования ниобия.
Металлические сплавы

Добавление ниобия в сплав увеличивает его прокаливаемость, то есть способность затвердевать при нагревании и последующем охлаждении. Таким образом, материал, содержащий ниобий, можно подвергать специальной термообработке.
Сродство ниобия к углероду и азоту способствует улучшению механических свойств сплава, повышая, например, механическую прочность и устойчивость к абразивному износу.
Эти эффекты полезны, поскольку они могут расширить промышленное применение сплава.
Например, сталь - это металлический сплав, состоящий из железа и углерода. Добавление ниобия в этот сплав может иметь преимущества для:
- Автомобильная промышленность: сделать автомобиль легче и устойчивее к столкновениям.
- Строительство: улучшает свариваемость стали и обеспечивает ковкость.
- Транспортная трубопроводная промышленность: Позволяет строить конструкции с более тонкими стенками и большим диаметром без ущерба для безопасности.
супер сплавы

Суперсплав - это металлический сплав с высокой устойчивостью к высоким температурам и механической прочностью. Сплавы, содержащие ниобий, делают этот материал полезным для производства авиационных турбин или производства энергии.
Преимущество работы при высоких температурах делает из суперсплавов высокоэффективные реактивные двигатели.
сверхпроводящие магниты

Сверхпроводимость ниобия приводит к тому, что соединения ниобий-германий, ниобий-скандий и ниобий-титан используются в:
- Сканер аппаратов МРТ.
- Ускорители элементарных частиц, такие как Большой адронный коллайдер.
- Обнаружение электромагнитного излучения и исследование космического излучения материалами, содержащими нитрит ниобия.
Оксиды
Другие области применения ниобия - оксиды, в основном Nb.2O5. Основное использование:
- оптические линзы
- Керамические конденсаторы
- датчики pH
- детали двигателя
- Ювелирные изделия
История и открытие ниобия
В 1734 году некоторые руды из личной коллекции Джона Уинтропа были вывезены из Америки в Англию, и эти предметы вошли в коллекцию Британского музея в Лондоне.
Присоединившись к Королевскому обществу, британский химик Чарльз Хэтчетт сосредоточился на исследовании состава руд, имеющихся в музее. Так в 1801 году он выделил химический элемент в форме оксида и назвал его колумбием, а руду, из которой он был извлечен, колумбитом.
В 1802 году шведский химик Андерс Густав Экеберг сообщил об открытии нового химического элемента и назвал его танталом, имея в виду сына Зевса в греческой мифологии.
В 1809 году английский химик и физик Уильям Хайд Волластон проанализировал эти два элемента и обнаружил, что они имеют очень похожие характеристики.
По этой причине с 1809 по 1846 год колумбий и тантал считались одним и тем же элементом.
Позже немецкий минералог и химик Генрих Роуз, исследуя колумбитовую руду, заметил, что в ней также присутствует тантал.
Роза обнаружила присутствие другого элемента, похожего на тантал, и назвала его Ниобием в связи с Ниобой, дочерью Тантала, из греческой мифологии.
В 1864 году шведу Кристиану Бромстранду удалось выделить ниобий из образца хлорида, нагретого в атмосфере водорода.
В 1950 году Союз чистой и прикладной химии (IUPAC) утвердил ниобий в качестве официального названия, а не колумбий, поскольку они были одним и тем же химическим элементом.
Резюме ниобия
Химический элемент: ниобий | |||
|---|---|---|---|
| Символ | Nb | Первооткрыватель | Чарльз Хэтчетт |
| атомный номер | 41 | атомная масса | 92 906 ю |
| Группа | 5 | Курс времени | 5 |
| Классификация | переходный металл | Электронная раздача | [Kr] 4d35 с2 |
| Функции |
|
||
| Основные руды |
|
||
| Основные продукты |
|
||
| Приложения |
|
||
| Вхождение | В мире |
|
|
| В Бразилии |
|
Упражнения врага и вступительные экзамены
1. (Enem / 2018) В греческой мифологии Ниобия была дочерью Тантала, двух персонажей, известных своими страданиями. Атомный номер химического элемента (Z), равный 41, по химическим и физическим свойствам настолько похож на атомный номер элемента 73, что их перепутали.
Поэтому в честь этих двух персонажей в греческой мифологии эти элементы получили названия ниобий (Z = 41) и тантал (Z = 73). Эти два химических элемента приобрели большое экономическое значение в металлургии, при производстве сверхпроводники и в других высокотехнологичных отраслях промышленности, именно из-за химических и физических свойств общий для обоих.
КИН, С. Исчезающая ложка: и другие правдивые истории о безумии, любви и смерти от химических элементов. Рио-де-Жанейро: Захар, 2011 (адаптировано).
Экономическое и технологическое значение этих элементов из-за схожести их химических и физических свойств обусловлено:
а) иметь электроны на f-подуровне.
б) являющиеся элементами внутреннего перехода.
в) принадлежат к той же группе в периодической таблице.
г) имеют свои внешние электроны на уровнях 4 и 5 соответственно.
д) принадлежать к семейству щелочноземельных и щелочных металлов соответственно.
Правильная альтернатива: в) принадлежат к той же группе в периодической таблице.
Таблица Менделеева разделена на 18 групп (семейств), каждая из которых объединяет химические элементы со схожими свойствами.
Это сходство происходит потому, что элементы группы имеют одинаковое количество электронов в валентной оболочке.
Выполняя электронное распределение и добавляя электроны с самого энергетического подуровня к самому внешнему подуровню, мы находим группу, к которой принадлежат эти два элемента.
| Ниобий | |
|
Распределение электроника |
1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p65 с2 4d3 |
|
сумма электроны |
более энергичный + более внешний 4d3 + 5 с2 = 5 электронов |
| Группа | 5 |
| Тантал | |
|
Распределение электроника |
1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 5 с2 4d10 5p66 с2 4f145d3 |
|
сумма электроны |
более энергичный + более внешний 5d3 + 6с2 = 5 электронов |
| Группа | 5 |
Элементы ниобий и тантал:
- Они принадлежат к одной группе в периодической таблице.
- У них самые внешние электроны находятся на уровнях 5 и 6 соответственно, и поэтому они расположены в 5-м и 6-м периодах.
- У них есть электроны на d-подуровне и, следовательно, они являются переходными элементами снаружи.
2. (IFPE / 2018) Бразилия - крупнейший в мире производитель ниобия, на долю которого приходится более 90% запасов этого металла. Ниобий, обозначенный символом Nb, используется в производстве специальных сталей и является одним из самых стойких металлов к коррозии и экстремальным температурам. Соединение Nb2O5 это предшественник почти всех сплавов и соединений ниобия. Отметьте альтернативу с необходимой массой Nb.2O5 чтобы получить 465 граммов ниобия. Дано: Nb = 93 г / моль и O = 16 г / моль.
а) 275 г
б) 330 г
в) 930 г
г) 465 г
д) 665 г
Правильная альтернатива: д) 665 г
Соединение-предшественник ниобия - оксид Nb.2O5 и ниобий, используемый в сплавах, находится в форме элементарного Nb.
Следовательно, мы имеем следующие стехиометрические отношения:
1 моль Nb2O5 образует 2 моля Nb, так как оксид ниобия образован 2 атомами этого металла.
1-й шаг: подсчитать количество произведенных молей ниобия, что соответствует 465 г.
Если расчетом мы увидели, что масса ниобия соответствует 5 молям, то количество молей Nb2O5 используется половина этого значения, потому что:
2-й шаг: вычислить молярную массу оксида ниобия.
3-й шаг: вычислить массу оксида ниобия, соответствующую 2,5 молям.
3. (UECE / 2015) Бразилия владеет 98% мировых запасов ниобия, который имеет множество промышленных применений, таких как, например, производство ювелирных изделий, гипераллергенные имплантаты, электрокерамика, сверхпроводящие магниты, магнитно-резонансные машины, металлические сплавы, специальные монеты и при производстве стали. Что касается ниобия, просмотрите приведенные ниже утверждения и отметьте единственно верную альтернативу.
а) Его дифференциальный электрон находится в предпоследней оболочке.
б) Это репрезентативный элемент.
в) Его электроотрицательность ниже, чем у ванадия.
г) Он принадлежит четвертому периоду таблицы Менделеева.
Правильная альтернатива: а) Его дифференциальный электрон находится в предпоследней оболочке.
При проведении электронного распределения ниобия можно увидеть, что его дифференциальный электрон находится в предпоследней оболочке.
Поскольку он имеет дифференциальный электрон на d-подуровне, он является внешним переходным элементом.
Поскольку его внешний уровень находится в пятом слое, ниобий находится в пятом периоде таблицы.
Электроотрицательность - это свойство, связанное со способностью элемента притягивать электроны, и оно варьируется в зависимости от атомный радиус: чем меньше атомный радиус, тем больше притяжение для электронов и, следовательно, тем больше электроотрицательность.
Просматривая таблицу со значениями электроотрицательности, можно увидеть, что ниобий и ванадий имеют значения, близкие к 1,6 по Полингу.
4. (UEA / 2014) Природным изотопом ниобия является 93Nb. Количество нейтронов в этом изотопе равно
а) 41.
б) 52.
в) 93.
г) 134.
д) 144.
Правильная альтернатива: б) 52.
Изотопы - это атомы химического элемента с разными массовыми числами.
Атомная масса соответствует сумме протонов и нейтронов элемента.
Число протонов представляет собой атомный номер химического элемента и для изотопов он не меняется.
Таким образом, изменение массы изотопов происходит из-за разного количества нейтронов.
Если атомный номер ниобия равен 41, то количество нейтронов определяется расчетом:
5. (IFMG / 2015) Химический элемент ниобий, Nb, назван в честь греческой богини Ниобы. Бразилия - крупнейший производитель металла в мире, на долю которого приходится 75% производства. Благодаря термостойкости сплавов ниобий используется в производстве специальных высокопрочных стальных сплавов для двигателей, силового оборудования и различных сверхпроводящих материалов. Наблюдая за положением ниобия в таблице Менделеева, правильно констатировать, что:
а) ваш самый энергичный подуровень будет подуровнем d.
б) представляет собой элемент, принадлежащий к семейству щелочных металлов.
в) образует ионные соединения с другими металлами.
г) его катионы будут иметь атомный радиус больше, чем чистый элемент.
Правильная альтернатива: а) ваш самый энергичный подуровень будет подуровнем d.
Посмотрев на таблицу Менделеева, мы можем увидеть, что ниобий характеризуется как внешний переходный элемент, который принадлежит к группе 5 Периодической таблицы, поскольку его самый энергетический подуровень - d.
Мы также можем получить эту информацию, распространяя ее в электронном виде.
Поскольку это металл, этот элемент создает металлические связи с другими металлами, как в сплаве. железо-ниобий или ковалентные связи за счет обмена электронами, как в оксиде ниобия Nb2O5.
6. (UFSC / 2003) Ниобий был открыт в 1801 году английским химиком Чарльзом Хэтчеттом. На Бразилию приходится около 93% мирового производства ниобиевого концентрата. Самые крупные месторождения находятся в штатах Минас-Жерайс, Гояс и Амазонас. Металл в основном используется в производстве сплавов железа с ниобием и других более сложных сплавов, которые применялись при создании турбин с реактивным двигателем, ракет и космических аппаратов. Его оксиды используются при производстве световых линз для очков, фотоаппаратов и другого оптического оборудования. Учитывая (Z = 41). Относительно ниобия отметьте ПРАВИЛЬНОЕ предложение (я).
(01) Ниобий, теряя 3 электрона, принимает конфигурацию криптона.
(02) Ниобий может образовывать оксиды металлов M-типа.2O5 в2O3.
(04) Химический символ ниобия - Ni.
(08) Ниобий - переходный металл.
(16) Сплав железа с ниобием является примером твердого раствора.
Правильные альтернативы: 02 + 08 + 16 = 26.
(01) НЕПРАВИЛЬНО.
| Элементы | Электронная раздача |
| 36Kr | 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 |
|
41Nb 41Nb3+ |
1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 5 с2 4d3 1 с2 2 с2 2p6 3 с2 3p6 4 с2 3d10 4p6 4p6 4d2 |
(02) ПРАВИЛЬНО
Учитывая степени окисления 3+ и 5+ для ниобия, он может образовывать соединения:
| Окислительное число 5+ | Число окисления 3+ |
| Nb2O5 | Nb2O3 |
(04) НЕПРАВИЛЬНО
Ni - это символ элемента никель. Символ ниобия - Nb.
(08) ПРАВИЛЬНО
Ниобий - это внешний переходный металл, принадлежащий к группе 5 Периодической таблицы.
(16) ПРАВИЛЬНО
Твердый раствор соответствует смеси двух или более компонентов в одной и той же фазе, которая является твердой, что является обычным явлением для металлов.
7. (UERJ / 2013) Ниобий - это металл, обнаруженный в природных месторождениях, в основном в форме оксидов.
В осадке, содержащем ниобий со степенью окисления +5, формула преобладающего оксида этого металла соответствует:
а) NbO5
б) Nb5O
в) Nb5O2
г) Nb2O5
Правильная альтернатива: d) Nb2O5
Кислород образует две связи и имеет фиксированную степень окисления, равную 2-.
Следовательно, для образования оксида ниобия кислород должен связываться с 2 атомами этого металла.
Ниобий имеет разные степени окисления. Со степенью окисления 3+ он связывается с 3 атомами кислорода, а с Nox 5+ образует соединение: Nb2O5 где 2 атома ниобия связаны с 5 атомами кислорода.
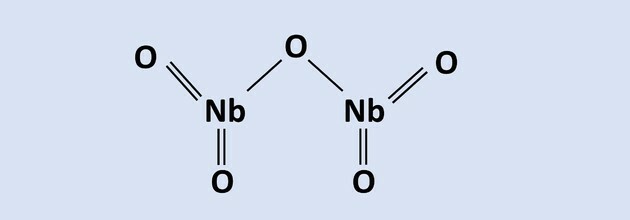
Прочтите текст, чтобы ответить на вопросы с 8 по 10.
Ниобий - металл, имеющий большое технологическое значение, и его основные мировые запасы находятся в
Бразилия, в виде пирохлорной руды, состоящей из Nb2O5. В одном из процессов экстрактивной металлургии используется алюминотермия в присутствии оксида железа.2O3, в результате чего получается сплав ниобия с железом и оксидом алюминия в качестве побочного продукта. Реакция этого процесса представлена уравнением:
В природе ниобий присутствует в виде стабильного изотопа ниобия-93, но известно несколько нестабильных синтетических изотопов, которые распадаются при испускании излучения. Один из них - ниобий-95, который распадается на элемент молибден-95.
(Systems.dnpm.gov.br; Технология Металл. Матер. Шахтер., Сан-Паулу, v. 6, вып. 4, стр. 185-191, апр.-июн. 2010 и Г. Ауди и др. / Ядерная физика A 729 (2003) 3–128. Адаптировано)
8. (FGV / 2019) В реакции алюминотермии для получения сплава ниобия и железа, учитывая стехиометрию, представленную в сбалансированном уравнении, общее количество электронов, участвующих в процессе, равно
а) 6.
б) 12.
в) 18.
г) 24.
д) 36.
Правильная альтернатива: д) 36.
Окислительно-восстановительная реакция происходит с потерей и приобретением электронов.
Когда элемент уменьшается, он получает электроны, а когда элемент окисляется, он теряет электроны.
Когда элемент восстанавливается, он является окислителем, а когда элемент окисляется, он является восстановителем.
Таким образом, количество электронов, которые были потеряны одним элементом и переданы другому, равно.
| Элемент | NOX | Реакция | электроны | |
| Ниобий |
+5 3Nb2O5 |
0 6Nb |
Снижение | 3.2.5 = 30 и- прибыль |
| Утюг |
+3 Вера2O3 |
0 2Fe |
Снижение | 2.3 = 6 и- прибыль |
| Алюминий |
0 12Al |
+3 6Al2O3 |
Окисление | 6.2.3 = 36 и- потерянный |
Заряд алюминия на продукте из оксида алюминия составляет 3+, то есть каждый алюминий потерял 3 электрона.
Но в изделиях у нас 12 атомов алюминия, что составляет общее количество электронов, участвующих в процессе:
12. 3 = 36 электронов.
9. (FGV / 2019) В алюминотермической операции по производству ниобия и сплава железа со стехиометрическими количествами Nb2O5 и Fe2O3 и из-за использования избыточного металлического алюминия образовалось 6,12 тонны алюминия.2O3. Общая сумма количеств в молях ниобия и железа, которые, по оценкам, будут получены в этой операции, составляет
а) 6 × 104
б) 6 × 106
в) 8 × 103
г) 8 × 104
д) 8 × 106
Правильный вариант: г) 8 × 104.
1-й шаг: вычислить молярную массу Al2O3
2-й шаг: вычислить количество молей Al2O3
3-й шаг: выполнить стехиометрические соотношения.
В химическом уравнении мы видим, что существует соотношение: 6 моль ниобия, 6 моль алюминия и 2 моль железа.
По соотношению количества образовавшихся молов имеем:
А сумма количеств ниобия и железа в молях составляет:
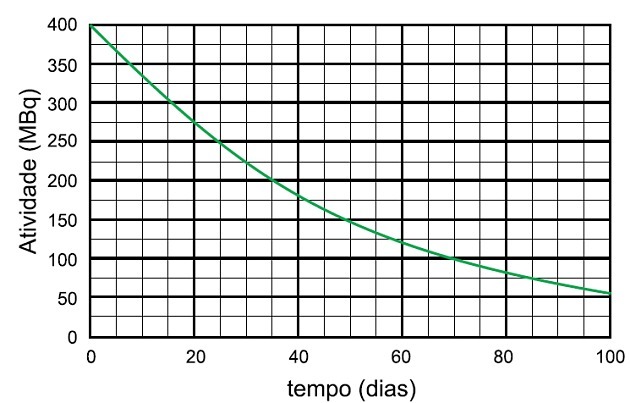
В процессе распада радиоизотопа ниобия-95 время, необходимое для того, чтобы активность этого образца снизилась до 25 МБк, и название испускаемого вещества равны
а) 140 суток и нейтронов.
б) 140 дней и протонов.
в) 120 дней и протонов.
г) 120 суток и частицы ß–.
д) 140 суток и частицы ß–.
Правильная альтернатива: д) 140 дней и частицы ß–.
Период полураспада - это время, за которое радиоактивный образец снижает свою активность вдвое.
На графике мы видим, что радиоактивная активность начинается с 400 МБк, поэтому период полураспада - это время, за которое активность снизилась до 200 МБк, что составляет половину от начальной.
Анализируем на графике, что на этот раз было 35 дней.
Чтобы активность снова упала вдвое, прошло еще 35 дней, и активность выросла с 200 МБк до 100 МБк, когда прошли еще 35 дней, то есть с 400 до 100 МБк прошло 70 дней.
Для распада образца до 25 МБк требовалось 4 периода полураспада.
Что соответствует:
4 x 35 дней = 140 дней
При радиоактивном распаде выбросы могут быть альфа, бета или гамма.
Гамма-излучение - это электромагнитная волна.
Альфа-излучение имеет положительный заряд и уменьшает на 4 единицы массы и на 2 единицы атомный номер распавшегося элемента, превращая его в другой элемент.
Бета-излучение - это высокоскоростной электрон, который увеличивает атомный номер распавшегося элемента на одну единицу, превращая его в другой элемент.
Ниобий-95 и молибден-95 имеют одинаковую массу, поэтому бета-излучение произошло по следующим причинам: