О стиральный порошок это чистящее средство, которое является частью повседневной жизни значительной части населения, поскольку оно используется для облегчения стирки одежды людей. Это продукт, пришедший на замену куску мыла, поскольку в процессе стирки у людей была привычка натирать им одежду.

Кусковое мыло по-прежнему широко используется при мытье посуды, например
Порошковое мыло было впервые произведено в 1946 году после нескольких попыток упростить использование кускового мыла. Одна из попыток заключалась в производстве мыла в виде хлопьев или гранул. Однако эти попытки не увенчались успехом, потому что мыло взаимодействует с ионами, присутствующими в жесткой воде, в основном ухудшая очищающее действие.
Почему нельзя так называть стиральный порошок?
С химической точки зрения мы не можем так называть стиральный порошок. Если мы посмотрим на упаковку этих продуктов, то увидим, что там написано стиральные машины, а не стиральный порошок. Это правильно называть Стиральный порошок, так как его химический состав отличается от состава мыла.
Химический состав стирального порошка или, лучше сказать, стирального порошка основан на принципиальной разнице между мылом и моющим средством. См. Определение и химические характеристики этих материалов:
а) Моющие средства:
Это химические вещества с очень длинными цепями (большое количество углерода). состоит только из атомов углерода и водорода, формируя то, что мы называем областями неполярный. Кроме того, в конце этой длинной цепочки находится полярная группа.
Полярная часть моющего средства обусловлена наличием сульфонатной группы, то есть атома серы, взаимодействующего с три атома кислорода или фосфатная группа, в которой атом фосфора взаимодействует с тремя атомами кислород. Смотрите изображение структуры моющего средства:
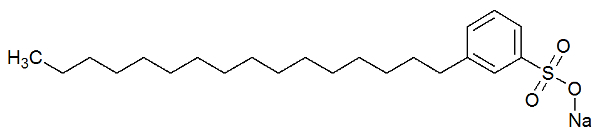
Структурная формула моющего средства
Полярная часть моющего средства (образованная сульфонатом натрия) способна взаимодействовать с молекулами воды. Неполярная часть (образованная только атомами углерода и водорода) взаимодействует с молекулами жира. Таким образом, моющее средство заставляет жир взаимодействовать с водой и образовывать эмульсию.
б) Мыло
соли карбоновые кислоты возникла в результате химической реакции между жирами и сильными основаниями, такими как NaOH. См. Изображение химической структуры мыла:
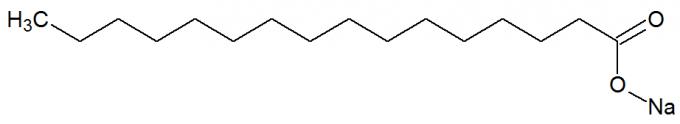
Структурная формула мыла
У них также есть длинные углеродные цепочки с неполярной и полярной частью. Таким образом, неполярная часть (состоящая только из атомов углерода и водорода) мыла может взаимодействовать с жиры и их полярная часть (образованная группой COONa) с водой образует эмульсии, например, моющие средства.
Поскольку в центре внимания этого текста находится химия «мыльного» порошка.или, точнее, химический состав порошкового моющего средства, мы представляем все химические вещества, входящие в его состав, а также важность каждого из них:
Химический состав порошкового моющего средства
анионное поверхностно-активное вещество (например, алкилбензолсульфонат натрия и сульфонат простого алкилового эфира натрия). Они связываются как с молекулой жира, так и с молекулой воды, таким образом удаляя жир из ткани;
Ферменты: Липазы и протеазы используются для удаления пятен. Это связано с тем, что с химической точки зрения ферменты являются биохимическими катализаторами, которые способствуют превращению сложных молекул в более простые. Таким образом, более мелкие молекулы легче удалить с одежды;
Отбеливатель (перборат натрия): Он действует путем окисления, восстановления или ферментативного действия. В воде он производит перекись водорода, которая является мощным окислителем. Они химически реагируют с пигментом одежды, модифицируя структуру и вызывая изменение цвета;
Оптические блокаторы: это вещества, которые поглощают ультрафиолетовое излучение или ультрафиолетовый свет и вскоре после этого излучают синий флуоресцентный свет, маскируя, например, желтоватый цвет одежды;
Ароматы: Это эссенции, которые оставляют на одежде приятный запах после стирки. Примечательно, что ароматы - это эссенции (они относятся к эфирной функции);
Красители: Вещества, используемые для окрашивания продукта;
Секвестрирующие и хелатирующие агенты: ЭДТА (этилендиаминтетрауксусная кислота) является примером секвестранта. Они взаимодействуют с ионами кальция, магния и железа, присутствующими в основном в жесткой воде, не допуская взаимодействия каких-либо компонентов очищающего действия, таких как поверхностно-активное вещество.
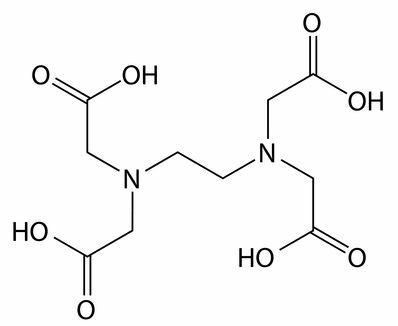
Структурная формула секвестранта ЭДТА
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/quimica-sabao-po.htm
