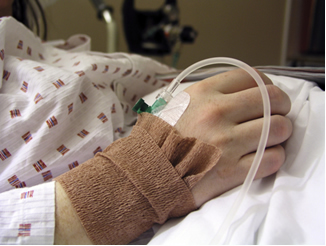
Графен - это наноматериал, состоящий только из углерода, в котором атомы соединяются вместе, образуя гексагональные структуры.
Это лучший из известных кристаллов, и его свойства делают его очень желанным. Этот материал легкий, проводящий электричество, жесткий и водостойкий.
Применимость графена находится в нескольких областях. Наиболее известны: гражданское строительство, энергетика, телекоммуникации, медицина и электроника.
С момента своего открытия графен остается центром исследовательского интереса. Изучение приложений для этого материала мобилизует учреждения и инвестиции в миллионы евро. Поэтому ученые всего мира продолжают пытаться разработать более дешевый способ массового производства.
Понимание, что такое графен
Графен - это аллотропная форма углерода, в которой расположение атомов этого элемента образует тонкий слой.
Этот аллотроп двухмерный, то есть имеет всего два измерения: ширину и высоту.
Чтобы получить представление о размерах этого материала, толщина листа бумаги соответствует наложению 3 миллионов слоев графена.
Хотя это самый тонкий материал, выделенный и идентифицированный человеком, его размер составляет порядка нанометров. Он легкий и прочный, способен проводить электричество лучше, чем такие металлы, как медь и кремний.
Расположение атомов углерода в структуре графена делает в нем очень интересные и желательные характеристики.
Приложения с графеном
Многие компании и исследовательские группы по всему миру публикуют результаты работы с приложениями для графена. Смотрите ниже основные из них.
| Питьевая вода | Мембраны, образованные графеном, способны опреснять и очищать морскую воду. |
|---|---|
| Выбросы CO2 | Графеновые фильтры снижают выбросы CO2 путем отделения газов, производимых промышленностью и предприятиями, которые будут отклонены. |
| обнаружение болезни | Гораздо более быстрые биомедицинские сенсоры основаны на графене и могут обнаруживать болезни, вирусы и другие токсины. |
| Строительство | Строительные материалы, такие как бетон и алюминий, становятся легче и прочнее с добавлением графена. |
| Красота | Окрашивание волос распылением графена, продолжительность которого составит около 30 стирок. |
| Микроустройства | Чипы стали еще меньше и прочнее за счет замены кремния графеном. |
| Энергия | Солнечные элементы с использованием графена обладают большей гибкостью, большей прозрачностью и более низкими производственными затратами. |
| Электроника | Батареи с улучшенным и быстрым накоплением энергии могут заряжаться до 15 минут. |
| Мобильность | Велосипеды могут иметь более прочные шины и рамы весом 350 граммов с использованием графена. |
Структура графена
Структура графена состоит из сети атомов углерода, соединенных в шестиугольники.
Ядро углерода состоит из 6 протонов и 6 нейтронов. 6 электронов атома распределены в два слоя.
В валентный слой есть 4 электрона, причем эта оболочка вмещает до 8. Следовательно, чтобы углерод приобрел стабильность, он должен образовать 4 соединения и достичь электронной конфигурации благородного газа, как указано в правиле октетов.
Атомы в графене связаны между собой ковалентные связи, то есть происходит обмен электронами.

Связи углерод-углерод являются самыми прочными связями, встречающимися в природе, и каждый углерод соединяется с тремя другими в структуре. Следовательно, гибридизация атома sp2, что соответствует 2 одинарным и одной двойной связи.
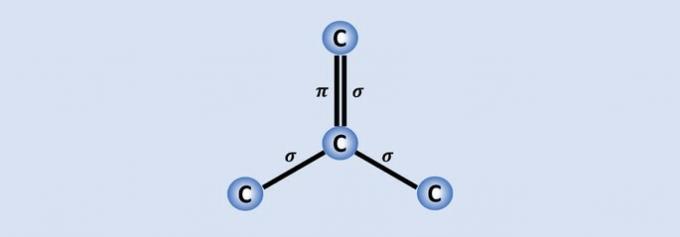
Из 4 электронов углерода три используются совместно с соседними атомами, а один составляет связь. , помогает графену, например, быть хорошим проводником электричества, потому что у него больше «свободы» в материале.
Свойства графена

| Свет | Квадратный метр весит всего 0,77 миллиграмма. Графеновый аэрогель примерно в 12 раз легче воздуха. |
|---|---|
| Гибкий | Он может расширяться до 25% своей длины. |
| Дирижер | Его плотность тока выше, чем у меди. |
| Прочный | Он расширяется на холоду и сжимается при нагревании. Большинство веществ действуют противоположным образом. |
| Водонепроницаемый | Сетка, образованная углеродом, не пропускает даже атом гелия. |
| Стойкий | Примерно в 200 раз прочнее стали. |
| Полупрозрачный | Поглощает всего 2,3% света. |
| Тонкий | В миллион раз тоньше человеческого волоса. Его толщина всего один атом. |
| Жесткий | Известный самый твердый материал, даже более твердый, чем алмаз. |
История и открытие графена
Термин графен впервые был использован в 1987 году, но официально был признан только в 1994 году União de Química Pure and Applied.
Это обозначение возникло от стыка графит с суффиксом -ene, относящимся к двойной связи вещества.
С 1950-х годов Линус Полинг говорил на своих занятиях о существовании тонкого слоя углерода, состоящего из шестиугольных колец. Филип Рассел Уоллес также описал некоторые важные свойства этой структуры несколькими годами ранее.
Однако только недавно, в 2004 году, графен был выделен физиками Андре Геймом и Константином Новоселовым в Университете Манчестера и стал широко известен.
Они изучали графит и, используя технику механического отслоения, смогли изолировать слой материала с помощью скотча. За это достижение пара получила Нобелевскую премию в 2010 году.
Важность графена для Бразилии
Бразилия обладает одними из самых больших запасов природного графита - материала, содержащего графен. Запасы графита составляют 45% от мировых.
Хотя наличие графита наблюдается на всей территории Бразилии, разрабатываемые запасы находятся в штатах Минас-Жерайс, Сеара и Баия.
Обладая богатым сырьем, Бразилия также инвестирует в исследования в этой области. Первая лаборатория в Латинской Америке, посвященная исследованиям графена, находится в Бразилии в Университете Пресбитериана Маккензи в Сан-Паулу и называется MackGraphe.
Производство графена
Графен можно получить из карбида, углеводорода, углеродных нанотрубок и графита. Последний является наиболее используемым в качестве исходного материала.
Основными методами производства графена являются:
- Механическое микроэксфолиация: Кристалл графита имеет слои графена, снятые с помощью ленты, которые нанесены на подложки, содержащие оксид кремния.
- Химическое микроэксфолиация: углеродные связи ослабляются добавлением реагентов, частично разрывая сетку.
- химическое осаждение из паровой фазы: формирование слоев графена, нанесенных на твердые носители, например на поверхность металлического никеля.
Цена графена
Сложность синтеза графена в промышленных масштабах означает, что ценность этого материала все еще очень высока.
По сравнению с графитом его цена в тысячи раз выше. Если 1 кг графита продается за 1 доллар, то продажа 150 г графена производится за 15 000 долларов.
Любопытства о графене
- Проект Европейского Союза, названный Графен Флагман, выделила около 1,3 миллиарда евро на исследования, связанные с графеном, приложениями и развитием производства в промышленных масштабах. В этом проекте участвуют около 150 учреждений в 23 странах.
- Первый чемодан, разработанный для космических путешествий, имеет в своем составе графен. Его запуск намечен на 2033 год, когда НАСА планирует провести экспедиции на Марс.
- Борофен - новый конкурент графена. Этот материал был обнаружен в 2015 году и считается улучшенной версией графена, поскольку он еще более гибкий, стойкий и проводящий.
Графен в Энеме
В тесте Enem 2018 один из вопросов Естественные науки и их технологии был о графене. Проверьте ниже прокомментированное решение этой проблемы.
Графен представляет собой аллотропную форму углерода, состоящую из плоского листа (двумерного массива) уплотненных атомов углерода толщиной всего в один атом. Его структура шестиугольная, как показано на рисунке.
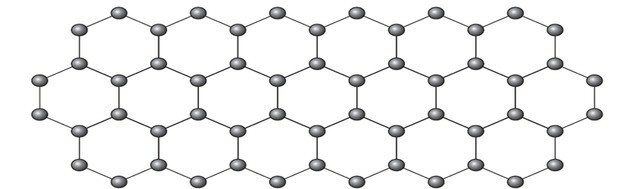
В этом расположении атомы углерода имеют гибридизацию
а) зр линейной геометрии.
б) зр2 плоской тригональной геометрии.
в) зр3 чередовались с sp-гибридизированными атомами углерода линейной геометрии.
г) зр3d плоской геометрии.
д) зр3d2 с гексагональной плоской геометрией.
правильная альтернатива: б) зр2 плоской тригональной геометрии.
Аллотропия углерода возникает из-за его способности образовывать различные простые вещества.
Поскольку он имеет 4 электрона в валентной оболочке, углерод четырехвалентен, то есть имеет тенденцию образовывать 4 ковалентные связи. Эти связи могут быть одинарными, двойными или тройными.
В зависимости от связей, которые образует углерод, пространственная структура молекулы изменяется на расположение, которое лучше всего вмещает атомы.
Гибридизация происходит, когда существует комбинация орбиталей, а для углерода это может быть: sp, sp.2 и зр3, в зависимости от типа звонков.
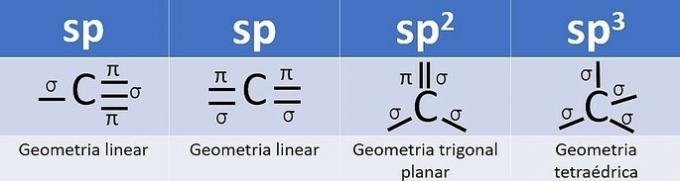
Число гибридных орбиталей - это сумма сигма (σ) -связей, которые образует углерод, поскольку связь не гибридизуется.
- sp: 2 сигма ссылки
- зр2: 3 сигма ссылки
- зр3: 4 сигма ссылки
Представление аллотропа графена в шариках и палочках, как показано на рисунке в вопросе, не демонстрирует истинных связей вещества.
Но если мы посмотрим на часть изображения, мы увидим, что есть один углерод, представляющий шар, соединенный с тремя другими атомами углерода, образующими структуру, подобную треугольнику.
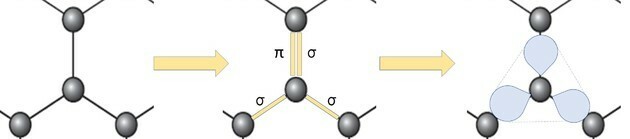
Если углерод нуждается в 4 связи и связан с 3 другими атомами углерода, то одна из этих связей является двойной.
Поскольку он имеет одну двойную и две одинарные связи, графен имеет sp-гибридизацию.2 и, следовательно, тригональная планарная геометрия.
Другие известные аллотропные формы углерода: графит, алмаз, фуллерен и нанотрубка. Хотя все они сделаны из углерода, аллотропы имеют разные свойства, обусловленные их разной структурой.
Тоже читай: Химия в Enem а также Вопросы по химии в Enem.