Ты оксиды они состоят из двух разных элементов, один из которых - кислород, который должен быть наиболее электроотрицательным из двух.
Номенклатура неорганических оксидов подчиняется правилам, которые зависят от того, является ли оксид молекулярным, ковалентным или ионным. Давайте рассмотрим каждый случай:
* Номенклатура молекулярных оксидов или ковалентной сетки:
Оксиды с молекулярной или ковалентной сеткой - это оксиды, в которых кислород присоединен к металл, такие как углерод (C), азот (N), сера (S), фтор (F) и другие. Номенклатура этих оксидов подчиняется следующему правилу:

Правило номенклатуры оксидов, образованных с помощью металлов
Приставка "моно" перед кислородно-связанным элементом является необязательной.
Например, у нас есть следующий молекулярный оксид: CO.
- Префикс, указывающий количество кислорода: 1 кислород: мононуклеоз;
- оксид;
- Префикс, указывающий количество атомов другого элемента: 1 углерод: мононуклеоз;
- Название элемента, связанного с кислородом: углерод.
Итак, ваше имя такое: CO = монооксид углерода или же монооксид углерода.
См. Другие примеры:
углекислый газ - CO2
Трехокись серы - SO3
Дихлор-гептоксид - Cl2О7
Окись азота - N2О
Трехокись азота - N2О3
Окись азота - НЕТ
Двуокись азота - НЕТ2
Пятиокись азота - N2О5
Диоксид кремния - SiO2
Пятиокись дифосфора - П2О5
Трехокись серы - SO3
* Номенклатура ионных оксидов:
Ионные оксиды - это оксиды, в которых кислород связан с металл, такие как железо (Fe), свинец (Pb), натрий (Na), кальций (Ca), серебро (Ag) и другие. Обычно электрический заряд кислорода равен -2.
Упомянутая номенклатура оксидов с молекулярной или ковалентной сеткой в настоящее время также применяется к оксидам металлов и считается официальной.. См. Несколько примеров:
Окись железа - FeO
Окись свинца - PbO
Диоксид свинца - PbO2
Диоксид триоксид - Fe2О3
Однако существует специальная номенклатура оксидов металлов, которая до сих пор широко используется. Он основан на валентности элемента, связанного с кислородом.
Если элемент имеет единая валентность, то есть, если существует только один способ связать кислород и образовать только один тип оксида, правило наименования будет иметь следующий вид:

Правило наименования одновалентных ионных оксидов
Примеры:
- Оксид натрия - Na2О
- оксид кальция - CaO
- Оксид калия - К2О
- оксид алюминия - Al2О3
- оксид серебра - Ag2О
Но есть также ионные оксиды, образованные элементами с более одной валентности. В этих случаях правило именования выглядит следующим образом:
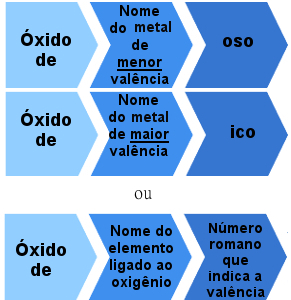
Правило номенклатуры для ионных оксидов с более чем одной валентностью
Примеры:
Оксид железа - FeO
Оксид железа - Fe2О3
Оксид меди - Cu2О
оксид меди - CuO
Или же:
Оксид железа II - FeO (NOx железа = +2)
Оксид железа III - Fe2О3 (NOx железа = +3).
Оксид меди I - Cu2O (NOx железа = +1)
Оксид меди II - CuO (NOx железа = +2).
Дженнифер Фогача
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm