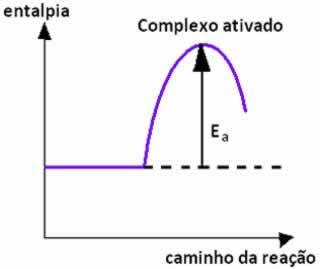
Уравновешенная обратимая реакция сместит свой баланс только в том случае, если произойдет какое-либо внешнее изменение, поскольку баланс никогда не сдвигается сам по себе.
Одним из таких изменений является изменение концентрации, которое включает удаление или добавление реагентов или продуктов.
Давайте посмотрим на пример:
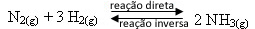
- Добавление реагентов:
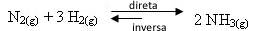
Если мы добавим больше газообразного водорода или больше газообразного азота к равновесию, концентрации реагентов увеличатся, а вместе с тем и количество эффективные удары между их молекулами также возрастут, что приведет к увеличению скорости развития прямой реакции образования аммиака. (NH3 (г)).
Это означает, что добавление реагентов смещает баланс в правую сторону, в сторону образования продуктов:

Это в соответствии с Принцип Ле Шателье который говорит, что когда в системе, находящейся в равновесии, возникает какое-то нарушение, она движется в направлении устранения этого нарушения, пытаясь приспособиться к новому равновесию.
В приведенном выше случае может случиться так, что со временем количество аммиака увеличится, снова достигнув равновесия. Таким образом, соотношение концентраций продуктов и реагентов останется постоянным, то есть значение константы равновесия Kc останется прежним.
Kc = __ [NH3]2__↑
[N2]. [ЧАС2]3 ↑
То же самое произойдет и в других случаях, то есть никакие изменения в концентрации реагентов или продуктов не повлияют на значение Kc.
- Добавление продуктов:
Если добавить больше аммиака, увеличивая его концентрацию, часть его превратится в газы. азот и водород, увеличивая скорость развития обратной реакции образования реагенты.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Это означает, что добавление продуктов смещает баланс влево, в сторону образования реагентов:
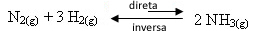
- Удаление реагентов:
Если удалить один или оба реагента, их концентрации уменьшатся и, как следствие, снизится скорость развития прямой реакции. Таким образом, баланс сместится в сторону образования большего количества реагентов, что находится влево:
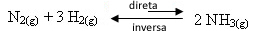
- Отзыв продукта:
Если мы уменьшим концентрацию продуктов, скорость обратной реакции будет уменьшаться, увеличивая скорость развития прямой реакции. Это означает, что баланс сместится вправо:
Вкратце можно сказать следующее:

Важно подчеркнуть, что изменение концентрации твердых веществ не нарушает равновесия.
Итак, в реакции ниже, если мы удалим или добавим CO2 (г) или CO(грамм), произойдет сдвиг баланса. Но если мы уменьшим или добавим C(s), с химическим балансом ничего не случится:
Ç(s) + CO2 (г) ↔ 2 CO(грамм)
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы ссылаться на этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Изменение концентрации и смещение химического равновесия»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/variacao-concentracao-deslocamento-equilibrio-quimico.htm. Доступ 28 июня 2021 г.