Анализ физических и химических свойств соединений, которые осуществляют ковалентные связи (путем обмена электронами), показывает нам, что между этими материалами есть большие различия. Но прежде чем мы посмотрим на сами эти характеристики, давайте посмотрим, в чем разница между молекулярными и ковалентными веществами.
В молекулярные вещества это те, которые образуются, когда атомы связаны ковалентными связями, давая начало молекулам определенного числа.
Однако ковалентная связь может также приводить к образованию соединений в сетчатой структуре с очень большим и неопределенным числом атомов, которые макромолекулы. Такие вещества называются ковалентные соединения или же твердые тела с ковалентной сеткой. Некоторые примеры этих соединений: алмаз (C), графит (C), диоксид кремния (SiO2) и карбид кремния (SiC).
Теперь давайте посмотрим на его основные свойства:
- Физическое состояние при комнатной температуре: В условиях окружающей среды обнаруживаются молекулярные и ковалентные соединения. в трех физических состояниях (твердое, жидкое и газообразное).
Примеры:
О Твердый: сахар (сахароза), кремнезем (песок), алмаз, графит;
О Жидкость: вода, ацетон, этанол;
О Газообразный: Сероводород, газообразный хлор, газообразный бром, газообразный водород.

- Температура плавления и кипения: В общем, температуры плавления и кипения этих веществ равны меньше, чем у ионных веществ.
Ковалентные вещества имеют более высокие температуры кипения, чем молекулярные, всегда выше 1000 ° C. Это связано с тем, что по мере того, как его молекулы более тесно связаны, образуя кристаллические решетки, необходимо подавать больше энергии, чтобы заставить их изменить свое состояние.
На температуру кипения и плавления ковалентных и молекулярных соединений влияют два фактора: молярная масса и межмолекулярная сила.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Чем больше молярная масса, тем больше инерция молекулы и, как следствие, выше температура кипения и плавления. Если молярные массы приблизительны, мы смотрим на межмолекулярные силы. Наиболее интенсивная межмолекулярная сила - это водородная связь, приводящая к более высокой температуре кипения и плавления. Промежуточным звеном является постоянный диполь, а самым слабым, что приводит к более низким температурам кипения и плавления, является индуцированный диполь.
- Электрический ток: В чистом виде ни жидкости, ни твердые тела не проводят электрический ток.
Исключением является графит, который проводит электрический ток в твердой форме, потому что его электроны с двойной связью резонируют и, следовательно, обладают определенной подвижностью.
- Растворимость: Поляры растворяются в полярах, а неполяры растворяются в неполярах.
- Упорство: Стойкость ковалентных веществ к ударам или механическим ударам невысока. Как правило, это хрупкие твердые вещества, как показано на примере стекла, которое образовано силикатами натрия и кальция.

- Прочность: В целом они обладают высокой твердостью. За исключением графита, потому что его атомы углерода связаны с тремя другими атомами углерода, образуя гексагональные пластины с определенной подвижностью, что делает его мягким. Из-за этого его даже используют как смазку.
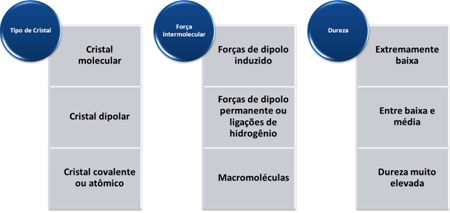
Твердость этих веществ варьируется в зависимости от типа кристалла, как показано в таблице ниже:
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы ссылаться на этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Свойства ковалентных и молекулярных соединений»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm. Доступ 28 июня 2021 г.
Ионные соединения, основные характеристики ионных соединений, связь между ионами, окончательный перенос электронов, силы электростатического притяжения между ионами, отрицательными и положительными ионами, анионами, катионами, ионной связью, молекулярной структурой он