Изомерия это естественное явление, при котором разные вещества (с точки зрения химических и физических свойств) имеют точно такую же молекулярную формулу, как в следующем примере:
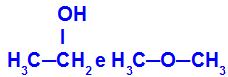
Различные вещества с одинаковой молекулярной формулой
Этанол (слева) имеет молекулярную формулу C2ЧАС6О, который также встречается с метоксиэтаном (справа), поэтому они являются изомерами.
Типы изомерии
→ плоский изомер
Это тип изомерии, изучающий структурные различия между изомерами.
) Занятие
Это тип плоской изомерии, в которой различие между веществами основано на различии органических функций, к которым они принадлежат. См. Несколько примеров:
Пропанон и пропан:
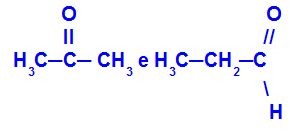
Изомеры, принадлежащие к разным функциям
Пропанон (слева) принадлежит к кетонной группе, а пропаналь (справа) принадлежит к альдегидной группе.
Б) Тюрьма
Это тип плоской изомерии, при которой различие между веществами основано на различии цепей, которые они представляют. См. Пример:
2-метилпропан и бутан
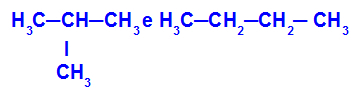
Изомеры с цепями разной классификации
В примере мы видим, что 2-метилпропан (слева) имеет разветвленную цепь, а бутан (справа) имеет нормальную цепь.
ç) Должность
Это тип плоской изомерии, при которой различие между веществами основано на различии положения компонента, присутствующего в их цепях. См. Пример:
1-хлорпропан и 2-хлорпропан
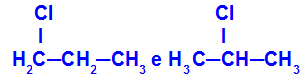
Изомеры, компоненты которых находятся в разных положениях в цепи.
В примере мы видим, что 1-хлорпропан (слева) имеет хлор, расположенный на углероде 1, а 2-хлорпропан (справа) имеет хлор, расположенный на углероде 2.
г) Метамерия или компенсация
ПРИМЕЧАНИЕ: Изомерия действительна исключительно для разнородных струн.
Это тип плоской изомерии, при котором различие между веществами основано на различии положения гетероатома, присутствующего в их цепях. См. Пример:
Пример: Метоксипропан и этоксиэтан
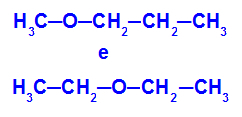
Изомеры с гетероатомами в разных положениях цепи
В примере мы видим, что в метоксипропане (слева) кислород имеет радикал с одним атомом углерода с одной стороны и тремя атомами углерода с другой. В этоксиэтане (справа) кислород имеет радикал с двумя атомами углерода с одной стороны и двумя атомами углерода с другой.
а также)Таутомеры
Это частный случай изомерии плоских функций, который встречается только в трех органических функциях:
Альдегид
кетон
Энол
Этот тип изомерии работает на том факте, что существует химический баланс между енолом и альдегидом и между енолом и кетоном, то есть эти компоненты постоянно превращаются друг в друга. См. Пример:
Проп-2-ен-1-ол и пропанон
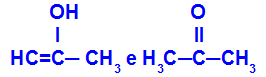
Изомеры, принадлежащие к разным функциям
В примере мы видим, что проп-2-ен-1-ол (слева) принадлежит к группе енолов, а пропанон (справа) принадлежит к группе кетонов, поэтому они являются изомерами таутомеров.
→ Космическая изомерия
Это тип изомерии, определяемый пространственным анализом молекулы.
а) Геометрические изомеры
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Это тип пространственной изомерии, которая возникает, когда вещество имеет молекулы со следующими характеристиками:
Замкнутая цепь с двумя атомами углерода с двумя разными лигандами, как в примере ниже:

Замкнутая структура с геометрической изомерией
Открытая цепь, которая имеет двойную связь между атомами углерода, и в каждом из этих атомов углерода двойной связи есть два разных лиганда, как в примере ниже:
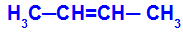
Открытая структура с геометрической изомерией
Геометрическая изомерия делится на две группы:
1O Группа: цис-транс
Это происходит, когда два лиганда одного углерода строго равны двум лигандам другого углерода, будь то в открытой или закрытой структуре.
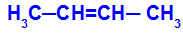
Цепь вещества, имеющего цис-транс-изомерию
Изомер будет называться цис, если одни и те же лиганды находятся в одной плоскости.

Пример цис-изомера
Изомер будет называться транс, если разные лиганды находятся в одной плоскости.

Пример транс-изомера
2O Группа: E-Z
Это происходит, когда два лиганда одного углерода отличаются по отношению к двум лигандам другого углерода, либо в открытой структуре, либо в закрытой структуре.

Цепочка вещества, имеющего изомерию E-Z
Изомер будет называться E, если лиганды с наивысшим атомным номером находятся в противоположных плоскостях. В приведенном ниже примере углерод слева имеет Br с наивысшим атомным номером (35), а в другом - кислород (8).
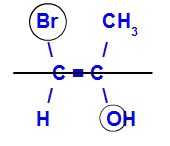
Пример E-изомера
Изомер будет называться Z, если лиганды с наивысшим атомным номером находятся в одной плоскости. В приведенном ниже примере углерод слева имеет Br с наивысшим атомным номером (35), а в другом - кислород (8).

Пример Z-изомера
Б) оптический изомер
Это тип пространственной изомерии, которая возникает только в том случае, если вещество имеет молекулы с хиральный углерод (тот, который имеет четыре разных лиганда) в их структурах. Молекула с хиральным углеродом обладает способностью поляризовать и отклонять свет следующим образом:
Справа (правый изомер)
Слева (левовращающий изомер)
Соединение с оптической активностью всегда имеет активные изомеры (называемые оптическими антиподами) и неактивные изомеры (смесь двух активных изомеров, смесь, называемая рацемической).
Мы можем использовать следующую формулу для определения количества активных (IOA) и неактивных (IOI) изомеров соединения, которое имеет хиральный углерод:
IOA = 2нет
IOI = 2нет
2
Ниже приведен пример соединения, имеющего геометрическую изомерию:
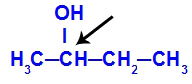
Хиральный углерод, содержащийся в бутан-2-оле
В состав бутан-2-ола входят следующие лиганды:
Метил (CH3)
Этил (CH3-CH2)
Водород (H)
Гидроксил (ОН)
Таким образом, бутан-2-ол имеет только один хиральный углерод, поэтому он имеет:
Активные изомеры:
IOA = 21
IOA = 2
Неактивные изомеры:
IOI = 21
2
IOI = 2
2
IOI = 1
Автор: Диого Лопес Диас
Хотели бы вы ссылаться на этот текст в учебе или учебе? Посмотрите:
ДНИ, Диого Лопес. «Что такое изомерия?»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria.htm. Доступ 27 июня 2021 г.
