Атомный номер, обозначаемый буквой Z, соответствует количеству протонов, существующих в ядре атома данного химического элемента. Например, атомный номер водорода равен 1, что означает, что в его атомном ядре есть только 1 протон.
Атомный номер обычно появляется слева от нижнего индекса химического элемента (в нижнем углу). Пример: 1ЧАС.
В основном состоянии атомный номер равен количеству электронов, так как в этом состоянии элемент нейтральный, поэтому количество положительных зарядов (протонов) должно равняться количеству отрицательных зарядов (электронов) атом.
Атомный номер важен, потому что именно он определяет основные характеристики и свойства элемента, а также его поведение и положение в Периодической таблице. Элементы перечислены в Периодической таблице в порядке возрастания атомного номера, который обычно отображается над элементом, как показано ниже. Обратите внимание, что первым элементом является водород H (Z = 1), затем идет гелий He (Z = 2), затем идет литий, Li (Z = 3) и так далее.
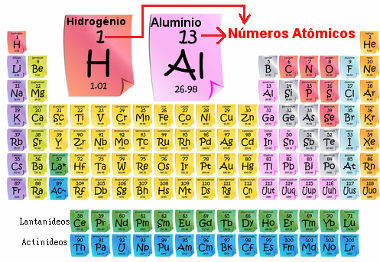
Атомный номер элементов в Периодической таблице
Мы даже можем представить себе химический элемент как «Набор атомов с одинаковым атомным номером». Таким образом, когда мы говорим, например, о химическом элементе кислороде, мы говорим об атомах с атомным номером 8. Ниже у нас есть атомы химических элементов из периодов 1 и 2 Периодической таблицы в порядке возрастания атомного номера:

Химические элементы из периодов 1 и 2 Периодической таблицы в порядке возрастания атомного номера
Атомные номера были первоначально определены английским физиком Генри Гвином Джеффрисом Мозли (1887-1915), и при проведении экспериментов по бомбардировке различными элементами Химики с рентгеновскими лучами, он заметил, что квадратный корень из частоты рентгеновских лучей, произведенных испусканием атомного ядра, прямо пропорционален атомному номеру элемента в таблице. Периодический. При этом он пришел к выводу, что атомный номер связан со свойствами атомов, потому что он представляет собой количество положительных зарядов в ядре каждого атома.
Химические связи не влияют на атомный номер атомов, поскольку в них участвуют только электроны, находящиеся в электросфере. Однако в ядерных реакциях участвует атомное ядро, и, следовательно, атомный номер также включен.
Например, когда частицы (в основном умеренные нейтроны) бомбардируют тяжелое нестабильное атомное ядро, это ядро разрушается и дает начало двум меньшим атомным ядрам, то есть с меньшим количеством протонов и нейтронов, высвобождая колоссальное количество энергия.
С другой стороны, ядерный синтез - это противоположный процесс, когда два небольших и легких ядра объединяются, образуя более крупное и более стабильное ядро, высвобождая еще большее количество энергии.
Таким образом, всякий раз, когда происходят эти ядерные реакции, возникают новые химические элементы, поскольку атомные номера исходных элементов отличаются от атомных номеров конечных элементов. Например, см. Ниже, что при делении урана-235 с атомным номером 92 образуются барий (Z = 56), криптон (Z = 36) и три нейтрона:

Реакция ядерного деления урана-235
Дженнифер Фогача
Окончила химический факультет
Источник: Бразильская школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-numero-atomico.htm
