Когда мы говорим о pH, мы имеем в виду гидрогенионный потенциал раствора, то есть количество катионов гидроксония (H+ или H3О+), которые диспергированы в растворителе раствора.
Катионы гидроксония хорошо известны благодаря определению, предложенному ученым. Архений для кислоты. Этот ученый утверждает, что кислота каждое вещество способно ионизировать и производят ионы гидроксония в водной среде.
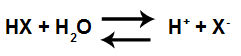
Уравнение ионизации кислоты
аббревиатура pH служит эталоном для определения уровня кислотности среды. Однако в течение долгого времени химики также использовали pH в качестве справочного материала для определения, помимо кислотности, является ли среда щелочной или нейтральной.
Это возможно, потому что теперь химики знают, что вода подвергается самоионизации, то есть производит гидроксоний (H+) и гидроксидов (OH-). Таким образом, водный раствор никогда не содержит только гидроксоний или гидроксид, но и то и другое, как мы можем видеть из следующего уравнения:

Уравнение автоионизации воды
Значения, используемые в качестве эталона для pH
Значения, используемые для pH относятся к константе ионизации (кВт) воды при температуре 25OC, что равно 10-14. При этой температуре концентрации ионов гидроксония и гидроксида, продуцируемых водой, абсолютно равны, то есть 10-7 Молл.
[ЧАС+] = [ОН-]= 10-7
Исходя из этой ссылки, значения, используемые для pH, находятся в диапазоне от 0 до 14.
Формулы для расчета pH
а) Расчет по концентрации катионов гидроксония в моль / л
Расчет значения pH можно выполнить напрямую, если нам известна концентрация гидроксониев ([H+]). Посмотрите:
pH = -log [H+]
или же
10-pH = [H+]
б) Расчет по концентрации гидроксид-анионов (OH-)
pOH = -log [OH-]
или же
10-pOH = [ОН-]
После расчета значения pOH вам необходимо использовать его в следующем выражении для определения значения pH.
pH + pOH = 14
Интерпретация значений pH
Зная значение pH, мы можем определить, имеет ли рассматриваемый раствор кислотный, щелочной или нейтральный характер. Для этого просто используйте следующие схематические отношения:
Для значений pH ниже 7 = кислая среда;
Для pH со значением 7 = нейтральная среда;
Для значений pH выше 7 = основная среда.
Примеры
1-й пример: Зная, что концентрация катионов гидроксония в растворе составляет 2,10-4 моль / л, какое должно быть значение pH этого раствора?
Для определения значения pH раствора по концентрации гидроксониев (H+), 2.10-4 моль / л, мы должны использовать следующее выражение:
pH = -log [H+]
pH = -log [2,10-4 ]
pH = - (log 2 + log 10-4)
pH = -log2 - log10-4
pH = –log 2 - 4.log 10
pH = –0,3 + 4. (1)
pH = -0,3 + 4
pH = 3,7
2-й пример: Раствор, образованный определенным растворенным веществом, имеет концентрацию гидроксид-иона, равную 10-11 Молл. Исходя из этой концентрации, мы можем сказать, сколько стоит pH этого раствора?
Чтобы определить значение pH раствора по концентрации гидроксида, 10-11 моль / л, мы должны сделать следующее:
1O Шаг: рассчитать значение pOH.
10-pOH = [ОН-]
10-pOH = 10-11
Мы должны умножить выражение на -1, потому что pOH всегда является положительным неизвестным.
-pOH = -11. (- 1)
pOH = 11
2O Шаг: рассчитать значение pH.
pH + pOH = 14
pH + 11 = 14
pH = 14-11
pH = 3
Автор: Диого Лопес Диас
Источник: Бразильская школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ph.htm

