THE Electrochimie este o ramură a chimiei fizice care studiază reacțiile în care există transfer de electroni (reacții de oxi-reducere) și ale acestuia conversia în energie electrică, precum și procesul opus, adică conversia energiei electrice în energie chimie.
Primul proces este ceea ce are loc în Baterii. Bateriile sunt dispozitive formate din doi electrozi (un pol pozitiv, care este catodul și un pol negativ, care este anodul), pe lângă un electrolit (soluție conductivă). Electronii sunt transferați de un conductor extern de la anod la catod, formând un curent electric care este utilizat pentru a porni un dispozitiv. Bateriile constau din mai multe celule conectate în serie sau în paralel.
Acesta este un proces spontan și energia este furnizată până la epuizarea reacției chimice (cum este cazul celulelor și bateriilor primare, cum ar fi celula uscată Leclanché și bateria alcalin), sau, în cazul reacțiilor reversibile, se poate aplica o diferență de potențial și reacția inversată, formând reactanții din nou și reîncărcând bateria care este gata de utilizare din nou (acesta este cazul bateriilor și bateriilor secundare, cum ar fi plumbul, utilizat în mașini și litiu-ion, utilizat în aparate celulare).

Bateriile și bateriile primare în prim-plan și, în al doilea, reîncărcarea bateriilor secundare (plumb și ion litiu)
Pe de altă parte, procesul invers nu este spontan și se numește electroliză. Electroliza este trecerea curentului electric care vine de la un generator, cum ar fi o celulă sau o baterie, printr-un lichid ionic. Dacă lichidul este o substanță topită, avem o electroliză magmatică, dar dacă este o soluție apoasă, avem o electroliza apoasă.
La trecerea curentului electric peste mediul lichid, generatorul „trage” electronii din polul pozitiv (anod - este opusul celui baterie) a celulei electrolitice și le transferă către polul negativ (catod), adică catodul suferă o reducere și anodul suferă oxidare. Astfel, energia electrică furnizată de generator este transformată în reacții redox (energie chimică). Mai jos este o schemă de electroliză a apei:
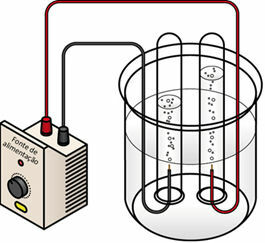
Schema de electroliză a apei
Electroliza se aplică pe scară largă industrial în producția de substanțe importante, precum aluminiu, clor gazos, sodiu metalic și pentru purificarea sau protejarea diferitelor metale, ca și în procedeele de galvanizare sau galvanizare, care constau în acoperirea unui obiect de către un metal, cum ar fi argintarea, placarea cu cupru, placarea cu nichel, aurirea și cromare; atunci când oțelul este acoperit cu zinc, se numește zincare.
În secțiunea din Electrochimie pe site-ul nostru veți găsi mai multe detalii despre toate aspectele legate de celule și baterii, precum și de electroliză.
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eletroquimica.htm
