În reacții de adițieîn alchene(hidrocarburi care au o legătură dublă între doi atomi de carbon), o legătură pi între doi atomi de carbon este ruptă și fiecare dintre atomi se atașează la un atom nou. Uite:
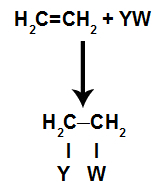
Model schematic general al unei reacții de adăugare
Principiile unei reacții de adăugare
a) Spargerea legăturii pi
O legătură pi este ușor de rupt, deoarece este o legătură mai slabă decât o legătură sigma. Cu toate acestea, pentru ca acest lucru să se întâmple, este necesar ca alchena să fie supusă unor condiții care asigură această perturbare. După ruperea legăturii pi dintre doi carboni, un site de legătură (pentru noi atomi) apare întotdeauna pe fiecare dintre carbonii implicați.
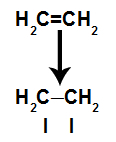
Schema care descrie ruperea legăturii pi
b) Condiții pentru ruperea unei legături pi
Factorii care favorizează ruperea unei legături pi sunt:
Utilizarea catalizatorilor;
Incalzi;
Prezența unui acid în mediul de reacție.
c) Apariția reacției de adăugare
Siturile de legare create după ruperea legăturii pi vor fi întotdeauna ocupate de atomi ai reactantului care se află în același recipient cu alchena. Reacția de adăugare este numită după tipul de reactiv amestecat cu alchena.
Tipuri de reacții de adăugare în alchene
a) Hidrogenare
O alchenă este amestecată cu hidrogen gazos (H2) într-un recipient și supus acțiunii unui catalizator solid (nichel, platină sau paladiu) și încălzire (Δ).
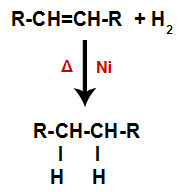
Schema generală a unei reacții de hidrogenare în alchene
Prezența catalizatorului și încălzirea provoacă legătura pi a alchenei și legătura sigma între hidrogenii H2 să fie rupt mai repede. Cu aceasta, avem crearea a două situri de legare în alchenă și a doi atomi de hidrogen liberi în mediul de reacție.

Crearea siturilor de legare și separare a atomilor
Astfel, imediat după aceea, fiecare atom de hidrogen liber ocupă unul dintre locurile de legătură formate în alchenă. Deoarece substanța formată are numai carboni și hidrogeni, precum și numai legături simple între carboni, este o alcan.
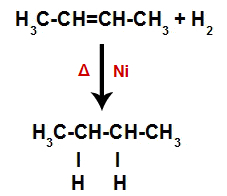
Ecuație reprezentând formarea alcanului în hidrogenare
B) Halogenare
O alchenă este amestecată cu substanțe simple (F2, Cl2, fr2 Hei2) format de halogeni (clor, fluor, iod și brom) într-un recipient și supus acțiunii luminii (λ) și încălzirii (Δ).

Schema generală a unei reacții de halogenare în alchene
Acțiunea luminii și încălzirea fac ca legătura pi a alchenei și legătura sigma dintre substanțele formate din halogen să se rupă mai repede. Cu aceasta, avem crearea a două situri de legare în alchenă și doi atomi de halogen liberi în mediul de reacție.

Crearea siturilor de legare și separare a atomilor
Astfel, imediat după aceea, fiecare atom de halogen liber ocupă unul dintre locurile de legătură formate în alchenă. Deoarece substanța formată are halogen legat de o structură compusă din carboni și hidrogeni, este o halogenură organică.

Ecuație reprezentând formarea de halogenuri organice în halogenare
c) Hidratare
O alchenă este amestecată cu apă (H2O) într-un recipient și supus acțiunii unui catalizator (în acest caz, acid sulfuric).
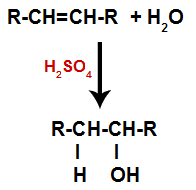
Schema generală a unei reacții de hidratare în alchene
Prezența acidului sulfuric în reacție face ca legătura pi a alchenei și legătura sigma dintre hidrogen (H) și hidroxil (OH) al apei să se rupă mai repede. Cu aceasta, avem crearea a două situri de legare în alchenă și un hidrogen liber și un hidroxil în mediul de reacție.
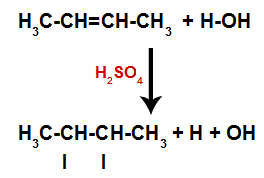
Crearea siturilor de legare și separare a atomilor
Astfel, la scurt timp după aceea, hidrogenul și hidroxilul ocupă unul dintre locurile de legătură formate în alchenă. Deoarece substanța formată are hidroxil legat de un carbon saturat (face doar legături simple), este un alcool.
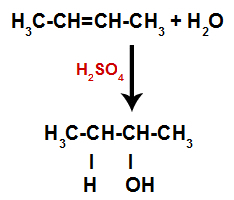
Ecuație reprezentând formarea alcoolului în hidratare
d) Adăugarea cu halogenuri de hidrogen
O alchenă este amestecată cu un acid anorganic halogenat (HF, HI, HCI, HBr) într-un recipient.

Schema generală a unei reacții cu halogenuri acide în alchene
Prezența acidului în reacție face ca legătura pi a alchenei să se rupă mai repede. Legătura unică din acid este ruptă deoarece aceste substanțe se ionizează în mod natural. Astfel, se creează două situri de legare în alchenă și există prezența unui hidrogen liber și a unui halogen în mediul de reacție.
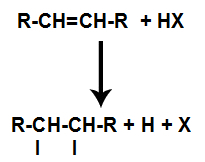
Crearea siturilor de legare și separare a atomilor
Astfel, la scurt timp după aceea, hidrogenul și halogenul ocupă unul dintre locurile de legătură formate în alchenă. Deoarece substanța formată are halogen legat de o structură compusă din atomi de carbon și hidrogen, este o halogenură organică.
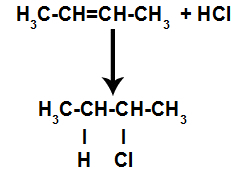
Ecuație reprezentând formarea de halogenuri organice în halogenare
De mine. Diogo Lopes Dias
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm

