sare dublă este numele dat uneia dintre clasificările pe care săruri anorganice poate primi. Celelalte clasificări sunt: simple, alaun, hidroxilat, hidrogenat și hidratat. Pentru a fi caracterizată ca o sare dublă, o sare anorganică trebuie să aibă una dintre combinațiile descrise mai jos:
Un cation (Y) și oricare doi anioni (X și W) și este reprezentat de următoarea formulă:
YXW
Un anion (X) și oricare doi cationi (Y și Z) și este reprezentat de următoarea formulă:
YZX
Notă: Aceste săruri se formează atunci când a reacție de neutralizare se efectuează între două baze diferit și unul acid, sau între doi acizi diferiți și o bază.
Regula de numire pentru o sare dublă
Pentru a numi un sare dublă, este necesar, mai întâi, să-i cunoaștem constituția, deoarece, pentru fiecare tip de sare dublă, există o regulă de denumire specifică, așa cum se poate vedea mai jos:
a) Regula nomenclaturii pentru sare dublă cu doi cationi
Când unul sare dublă are doi cationi, trebuie să folosim următoarea regulă:

Regula nomenclaturii utilizată pentru sărurile duble cu doi cationi
Următoarele sunt două exemple de aplicare a acestei reguli de denumire:
Primul exemplu: Linia4s
Această sare este compusă din:
Anion: sulfură (S-2);
Cation mai electropozitiv: litiu (Li+1);
Cationi mai puțin electropozitivi: amoniu (NH4+1).
Prin urmare, numele său este sulfură de litiu (dublu) de amoniu.
Al 2-lea exemplu: RbCaBO3
Această sare este compusă din:
Anion: borat (BO3-3);
Cation mai electropozitiv: rubidiu (Rb+1);
Cationi mai puțin electropozitivi: calciu (Ca+2).
Astfel, numele său este borat (dublu) de rubidiu și calciu.
b) Regula nomenclaturii pentru sare dublă cu doi anioni
Când unul sare dublă are doi anioni, trebuie să folosim următoarea regulă:
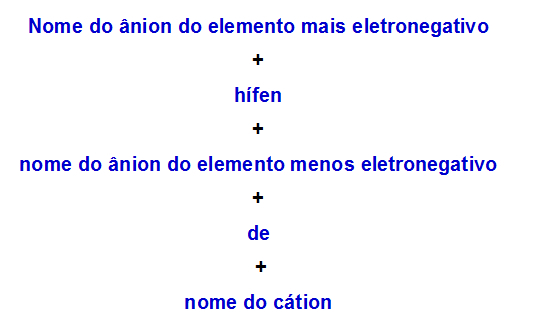
Regula nomenclaturii utilizată pentru sărurile duble cu doi anioni
Iată două exemple de aplicare a acestei reguli:
Primul exemplu: MgFI
Această sare este compusă din:
Cation: magneziu (Mg+2);
Cel mai mult anion electronegativ: fluor (F-1);
Anion mai puțin electronegativ: iodură (I-1).
Prin urmare, numele său este fluorură-iodură de magneziu.
Al 2-lea exemplu: ZnNO2fr
Această sare este compusă din:
Cation: zinc (Zn+2);
Anion mai electronegativ: nitrit (NO2-1);
Anion mai puțin electronegativ: bromură (Br-1).
Prin urmare, numele său este nitrit-bromură de zinc.
Asamblarea formulei de sare dublă din nomenclatura sa
a) Pentru sare dublă cu doi cationi
Construcția formulei a sare dublă depinde de cunoașterea numelui său, care este standardizat ca în toată sarea, adică mai întâi cationul și apoi anionul. Deoarece sarea dublă poate avea doi cationi, ordinea și plasarea lor în formulă urmează denumirii date.
Primul exemplu: pirofosfat de nichel de bariu II
Această sare conține fosfat (P2O7), bariu (Ba+2) și nichel II (Ni+2), cationi scrise în acea succesiune. Deci formula sa este BaNiP2O7.
Al 2-lea exemplu: fosfat de cupru II și aur I
Această sare are fosfat (PO4-3), cupru II (Cu+2) și aur I (Au+1), cationi scrise în acea succesiune. Prin urmare, formula sa este CuAuPO4.
b) Pentru sare dublă cu doi anioni
In caz de sare dublă cu doi anioni, urmăm, de asemenea, atunci când plasăm anionii în formulă, ordinea așa cum apar în numele dat.
Primul exemplu: sulfat de nichel-iodură III
Această sare are anioni sulfat (SO4-2) și iodură (I-1), scris în această succesiune, și cationul nichel III (Ni+3). Deci formula sa este NiSO4I.
Al 2-lea exemplu: fosfat de cianură de plumb IV
Această sare are anioni fosfat (PO4-3) și cianură (CN-1), scris în această succesiune, și cationul de plumb IV (Pb+4). Deci formula sa este PbPO4CN.
De mine. Diogo Lopes Dias
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm


