Reacțiile de halogenare sunt un tip de reacție de substituție organică, adică cele în care a atomul sau grupurile de atomi sunt înlocuiți cu atomi sau grupuri de atomi ai altei molecule organic.
În general, acest tip de reacție are loc cu alcani și hidrocarburi aromatice (benzen și derivații săi).
Halogenarea se numește așa deoarece apare cu substanțele simple ale halogenilor: F2, Cl2, fr2 Hei2. Cu toate acestea, cele mai frecvente dintre acestea sunt clorarea (Cl2) și bromurare (Br2), deoarece fluorul este foarte reactiv, iar reacțiile sale sunt explozive și greu de controlat, chiar distrugând materia organică:
CH4 (g) + 2 F.2 (g) → C(s) + 4HF(g)
Reacțiile cu iodul sunt extrem de lente.
Mai jos sunt principalele tipuri de halogenare și câteva exemple:
1. Halogenare cu alcani: Deoarece alcanii sunt slab reactivi, reacțiile lor de halogenare au loc numai în prezența razelor solare (λ), a luminii ultraviolete sau a încălzirii puternice. Acest tip de reacție se face pentru a obține o halogenură de alchil.
Exemplu: monoclorurarea metanului:
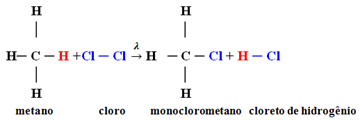
În acest caz a apărut dintr-un atom de hidrogen de metan (CH4) să fie înlocuit cu un atom de clor, dând monoclorometan. Dacă ar fi prea mult clor, această reacție ar putea continua să se proceseze, înlocuind toți hidrogenii din metan.
1.1. Halogenare în alcani cu mai mult de 3 atomi de carbon: Dacă alcanul care urmează să fie reacționat are cel puțin 3 atomi de carbon, vom ajunge cu un amestec de diferiți compuși substituiți. A se vedea exemplul de mai jos al unei monoclorurări cu metilbutan:
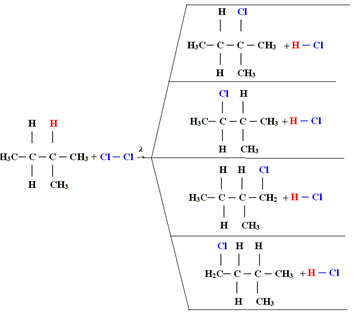
Cantitatea fiecărui compus va fi proporțională cu următoarea ordine de ușurință cu care hidrogenul este eliberat în moleculă:

Astfel, în cazul de mai sus, cea mai mare cantitate va fi 2-metil-2-clorobutan și cea mai mică cantitate va fi 2-metil-1-clorobutan.
2. Halogenare cu benzen: Benzenul nu reacționează în mod normal cu clorul sau bromul. Cu toate acestea, dacă se folosește un acid Lewis ca catalizator (de obicei se folosește FeCl3, FeBr3 sau AlCl3, toate sub formă anhidră), benzenul reacționează ușor într-o reacție de halogenare.
Clorura și bromura ferică pot fi obținute doar prin adăugarea de fier în amestec și în acest fel reacționează cu halogenul și produce acidul Lewis:
2 Fe + 3 Br2 → 2 FeBr3
Vezi un exemplu de halogenare a benzenului și mecanismul său:
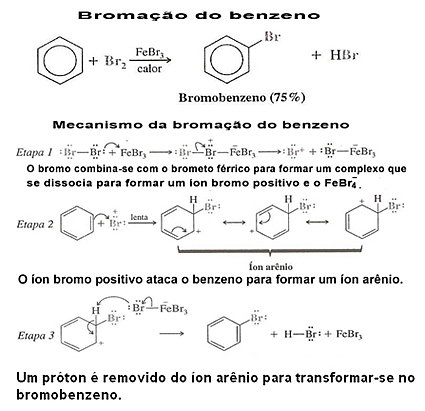
3. Halogenarea derivaților benzenici:În aceste cazuri, substituția este ghidată de substituent sau grupul funcțional care este atașat la nucleul aromatic. Pentru a vedea cum se întâmplă acest lucru, citiți textele "Radicalii de direcție în inelul benzenic" și "Efecte electronice ale radicalilor meta și orto-către-regizori”.
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm

