Reacțiile de oxidare-reducere studiate în principal în chimia fizică sunt cele în care are loc transferul de electroni. Specia care reacționează (atom, ion sau moleculă) care pierde unul sau mai mulți electroni este cea care suferă oxidare. Pe de altă parte, specia chimică care primește electroni este redusă.
În general, atunci când acest tip de reacție este studiat în chimia anorganică, se numește reacție de schimb simplă sau de deplasare.
Pentru ca orice reacție să aibă loc este necesar să se îndeplinească anumite condiții. Una dintre ele este că trebuie să existe afinitate chimică între reactivi, adică trebuie să interacționeze în așa fel încât să permită formarea de substanțe noi.
În cazul reacțiilor redox, afinitatea înseamnă că unul dintre reactanți tinde să câștige electroni, iar celălalt tinde să piardă electroni. Această tendință corespunde reactivitate a elementelor chimice implicate.
Să vedem cum este posibil să comparăm reactivitatea dintre metale.
Să presupunem că dorim să stocăm o soluție de sulfat de cupru II (CuSO
4). Nu am putut pune această soluție într-un recipient din aluminiu, deoarece ar avea loc următoarea reacție:2 Al(s) + 3 CuSO4 (aq)→ 3 Cu(s) + Al2(NUMAI4)3 (aq)
Rețineți că aluminiul s-a oxidat, pierzând 3 electroni fiecare și devenind cation de aluminiu:
Al(s) → Al3+(Aici) + 3 și-
Simultan, cationul de cupru (Cu2+) care a fost prezent în soluție a primit electroni din aluminiu și s-a redus, devenind cupru metalic. Fiecare cation de cupru primește doi electroni:
Cur2+(Aici) + 2 și- → Cu(s)
Cu toate acestea, dacă ar fi invers și am vrea să depozităm o soluție de sulfat de aluminiu (Al2(NUMAI4)3 (aq)), nu ar fi o problemă să-l puneți într-un recipient de cupru, deoarece această reacție nu ar avea loc:
Cur(s) + Al2(NUMAI4)3 (aq) → Nu se produce
Aceste fapte observate pot fi explicate prin faptul că aluminiul fiind mai reactiv decât cuprul.
Metalele au tendința de a renunța la electroni, adică de a se oxida. Când se compară diferite metale, cel cu cea mai mare tendință de a dona electroni este cel mai reactiv. În consecință, reactivitatea metalelor este, de asemenea, asociată cu a acestora energie de ionizare, adică energia minimă necesară pentru a îndepărta un electron din atomul gazos în starea sa fundamentală.

Pe baza acestui fapt, coadă de reactivitate metalică sau rând de tensiuni electrolitice, prezentat mai jos:
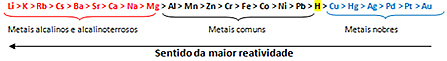
Cel mai reactiv metal reacționează cu substanțe ionice ale căror cationi sunt mai puțin reactivi. Cu alte cuvinte, metalul din stânga reacționează cu substanța formată din ioni din dreapta sa. Opusul nu se întâmplă.
Amintindu-ne de exemplul dat, vedeți în rândul de reactivitate că aluminiu (Al) este la stânga cuprului (Cu). Prin urmare, aluminiul reacționează cu soluția formată din cationi de cupru; dar cuprul nu reacționează cu o soluție formată din cationi de aluminiu.
Rețineți că cel mai reactiv metal este litiul (Li) și cel mai puțin reactiv este aurul (Au).

Acesta este unul dintre motivele pentru care aurul este atât de valoros, deoarece dacă nu reacționează, rămâne intact mult timp. Acest lucru poate fi văzut în sarcofagele și sculpturile egiptene acoperite cu aur care datează din cea mai îndepărtată antichitate. Vedem acest lucru și atunci când comparăm durabilitatea unei bijuterii din aur pur cu bijuteriile realizate din alte metale care sunt mai reactive decât aurul.

De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-metais.htm
