Oxizii acizi sunt acei oxizi care, atunci când reacționează cu apa, produc un acid ca produs. Când reacționați cu o bază, produsele vor fi sare și apă.
Acești compuși au de obicei un caracter covalent, adică sunt moleculari, solubili în apă și formați în mare parte din nemetale, care sunt elemente cu electronegativitate ridicată. Când sunt formate din metale, acestea au un număr mare de oxidare (încărcare electrică).
Exemple:
CO2, NUMAI2, NUMAI3, P2O5, Cl2O6, LA2, Nu2O4, Nu2O5, etc.
Următoarea este o schemă generală a reacțiilor caracteristice pentru oxizii acizi și un exemplu:
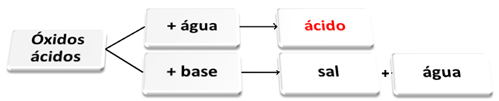
Oxizi acizi care reacționează cu apa și cu baza
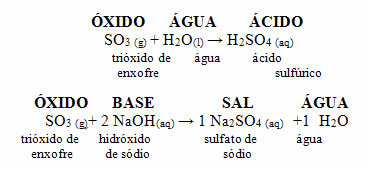
Oxizii acizi se mai numesc anhidridele, deoarece acest cuvânt provine din greacă anhidro, care înseamnă "fara apa", iar oxizii acizi pot fi considerați un „acid fără apă”.
Proprietăți și aplicații ale unor oxizi acizi:
• Dioxid de carbon (dioxid de carbon) - CO2:
Acest compus este utilizat ca gaz în băuturile răcoritoare și în apele minerale, deoarece atunci când este supus unei presiuni ridicate, devine solubil în apă. Produce în aceste produse un mediu acid, deoarece este un oxid acid care reacționează cu apa, producând un acid, conform reacției de mai jos:

Sub 78 ° C, se află într-o stare solidă și este cunoscută sub numele de gheață uscată, care își primește numele deoarece aspectul său seamănă cu gheața. comun, dar nu se topește, trecând la starea lichidă la temperatura camerei, dar trece la starea de vapori, adică sublimi. Astfel, această caracteristică este utilizată ca resursă scenică în concerte, filme, teatre, petreceri etc.

Dioxidul de carbon este un oxid acid
Se găsește și în atmosferă ca urmare a respirației umane, a arderii combustibililor fosili (cărbune, produse petroliere, alcool etc.) și a incendiilor forestiere. Astfel, el este unul dintre cei responsabili de ploile acide.
• Oxizi de sulf - SO2 Așadar3
Acești oxizi sunt prezenți și în atmosferă, fiind de origine naturală și artificială. Naturalul se produce prin erupții vulcanice și descompunerea plantelor și animalelor. Artificialul corespunde celei mai mari cantități de oxizi din atmosferă, așa cum sunt expulzat prin arderea combustibililor fosili, în principal motorină, care conține sulf precum impuritate.
Dioxid de sulf (SO2) reacționează cu oxigenul din atmosferă producând trioxid de sulf (SO3). Când acest ultim oxid reacționează cu apa de ploaie, se formează acid sulfuric, care este foarte puternic și provoacă daune.
• Arderea sulfului din combustibili: S + O2 → OS2
• Transformarea SO2 în SO3: SO2 + ½2 → OS3
Reacțiile SO2 și SO3 cu apă care dau acizi: SO2 + H2O → H2NUMAI3
NUMAI3 + H2O → H2NUMAI4
• Tetroxizi dinitrogeni (anhidridă azotată) - N2O4
Acest compus are un punct de fierbere de 22 ° C, are o culoare galbenă și este destul de volatil. Se formează în atmosferă prin oxidarea azotului și poate fi sub formă lichidă, sub forma unui dimer de dioxid de mononitrogen sau oxid nitric (NO2). Peste această temperatură, ia forma NO2:
N2O4 ↔ NU2
Este un gaz extrem de toxic și inhalarea acestuia este fatală. Este, de asemenea, utilizat în compoziția combustibililor pentru rachete.
De Jennifer Fogaça
Absolvent în chimie