A sublimare Este o schimbare a stării fizice a materiei caracterizată prin trecerea directă din faza solidă în faza gazoasă, fără a trece prin faza lichidă. Strict vorbind, orice substanță poate suferi sublimare, dar în condiții specifice de presiune și temperatură. Sublimarea este corelată cu presiunea vaporilor în faza solidă, precum și cu interacțiunile intermoleculare exercitate de solide.
Acest proces poate fi observat cu ușurință într-o bucată de gheață carbonică, care constă din dioxid de carbon solid. Dioxidul de carbon se sublimează sub presiune și la temperatura camerei. Procesul opus sublimării poate fi numit resublimare sau depunere. Pentru ca sublimarea să aibă loc, materia trebuie să absoarbă energie, deci este considerat un proces endotermic.
Citeste si: Care sunt stările fizice ale materiei?
Subiectele acestui articol
- 1 - Rezumat despre sublimare
- 2 - Ce este sublimarea?
-
3 - Operațiunea de sublimare
- Ce este presiunea vaporilor?
- Presiunea vaporilor și sublimarea
- Diagrama fazelor
- 4 - Exemple de sublimare
- 5 - Exerciții rezolvate de sublimare
Rezumat despre sublimare
Sublimarea este trecerea directă de la faza solidă la faza gazoasă, fără a trece prin faza lichidă.
Condiții specifice de presiune și temperatură sunt necesare pentru a observa sublimarea unei substanțe.
Sublimarea este influențată de aspecte termodinamice, cum ar fi presiunea vaporilor în faza solidă și interacțiunile intermoleculare.
Sublimarea este un proces endotermic.
Un exemplu de sublimare este ceea ce se întâmplă în gheața carbonică, care constă din dioxid de carbon solid.
Ce este sublimarea?
sublimarea este trecerea directă de la faza solidă la faza gazoasă, fara a trece prin faza lichida. Apare în condiții specifice de temperatură și presiune pentru unele solide. Această tranziție este un proces fizic de schimbare a stării, care nu implică reacții chimice.
Procesul invers, adică trecerea directă de la faza gazoasă la faza solidă, este denumit diferit. Unii autori păstrează cuvântul sublimare pentru această schimbare de fază, în timp ce alții folosesc „resublimare” și chiar „depunere”.
Nu te opri acum... Mai sunt dupa publicitate ;)
Cum funcționează sublimarea
Se poate face o paralelă între sublimare și evaporare. În ambele cazuri, punctul final este fază gazoasă. Diferența, evident, este în faza de pornire: solid pentru sublimare și lichid pentru evaporare.
În ambele cazuri, există influența presiunii devapor și, de asemenea, aspecte termodinamice, implicând căldură și interacțiuni intermoleculare.
Ce este presiunea vaporilor?
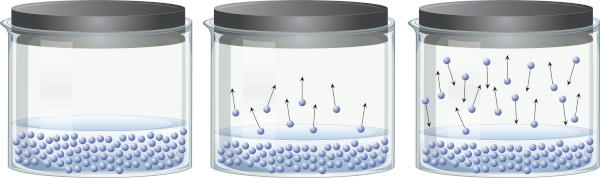
Într-un recipient închis care conține un lichid, este posibil să se perceapă că există un echilibru între faza lichidă și faza de vapori. Acest lucru se întâmplă deoarece, chiar și sub temperatura de fierbere, energia prezentă este suficientă pentru ca unele molecule de lichid să se desprindă și să treacă în vapori. Cu toate acestea, unele molecule de vapori se pot condensa din nou și se pot întoarce în faza lichidă, ceea ce demonstrează reversibilitatea procesului.
Acest vapor, fiind alcătuit din materie (are masă și volum), exerciții presiunea pe suprafața lichidului, cunoscută sub denumirea de presiune a vaporilor. Este dependentă nu de cantitatea de lichid, ci de temperatură, deoarece cu cât temperatura este mai mare, cu atât moleculele se desprind mai ușor din faza lichidă.
Lichidele care au o presiune mare a vaporilor la temperaturi obișnuite sunt numite volatile. De exemplu, la 25°C, eterul etilic are o presiune de vapori de 0,58 atm, acetona (propanona) are o presiune de vapori de 0,29 atm, în timp ce apa are o presiune de vapori de 0,023 atm. Apropo, atunci când presiunea vaporilor este identică cu presiunea atmosferică, lichidul fierbe. Pentru a afla mai multe despre presiunea vaporilor, faceți clic Aici.
Presiunea vaporilor și sublimarea
Deși într-o măsură mai mică, solidele au și presiunea vaporilor, dar mult mai mică decât cea a lichidelor. De exemplu, chiar și la o temperatură de 1000 K, presiunea de vapori a fierului este de numai 9,21 x 10-20 ATM. Cu toate acestea, unele solide reușesc să sufere sublimare, cum ar fi iodul, prezentând o presiune de vapori mai mare la temperaturi normale (4 x 10).-4 ATM).
Acest lucru este posibil numai cu trecerea moleculelor din starea solidă direct în starea gazoasă. Pentru ca acest lucru să se întâmple, moleculele solidului trebuie să prezinte interacțiuni intermoleculare slab (în iod, de exemplu, sunt de tip dipol indus de dipol).
Se vede si ca procesul de sublimare este endotermic, adică este nevoie ca moleculele solidului să absoarbă energie sub formă de căldură, astfel încât să poată rupe interacțiunile intermoleculare și să treacă în starea de vapori. Cantitatea de căldură implicată poate fi măsurată printr-o mărime termodinamică cunoscută sub numele de entalpia de sublimare.
Diagrama fazelor
La pentru a ști în ce interval de presiune și temperatură va avea loc sublimarea unui solid, trebuie să vă evaluați diagrama de fază. Să ne uităm la cazul dioxidului de carbon, CO2.

Într-o diagramă de fază, liniile de delimitare dintre stări (solid, lichid și gaz) reunesc valorile presiunii și temperaturii pentru are loc o schimbare de stare. La observarea cazului CO2 se observă că la 1 atmosferă de presiune, faza solidă trece direct în faza de vapori la o temperatură de -78,5 °C, ceea ce caracterizează o sublimare.
Dioxidul de carbon are doar fază lichidă la presiuni de peste 5,11 atmosfere, iar dincolo de această presiune, sublimarea nu mai este posibilă. Pentru a afla mai multe despre diagrama de fază, faceți clic Aici.
exemple de sublimare
Gheata uscata: gheața carbonică, folosită adesea pentru a produce efecte de ceață la petreceri și evenimente, este de fapt dioxid de carbon în stare solidă.

naftalină: naftalină sunt făcute din naftalină, un compus organic aromat. Se aplică pentru a îndepărta mirosurile neplăcute și, de asemenea, pentru a speria moliile, gândacii și alte animale veninoase, motiv pentru care este obișnuit ca acestea să fie folosite în dulapuri sau chiar în pisoare.

Camfor: Cu un miros caracteristic, pietricelele de camfor pot suferi și sublimare. De asemenea, servesc pentru a speria tantarii si pentru a preveni mucegaiul.

Iod: nemetalul aparținând halogenilor suferă și el sublimare.

Cu toate acestea, dintre substanțele prezentate, numai dioxidul de carbon suferă sublimare în condiții ambientale. Ceilalți, chiar și cu sublimare, pot suferi fuziunea normală sub presiunea în care trăim.
Citeste si: Plasma - a patra stare a materiei
Exercitii rezolvate de sublimare
intrebarea 1
(Fuvest 2020) În supermarketuri, este obișnuit să găsiți așa-numitele alimente liofilizate, cum ar fi fructele, legumele și carnea. Alimentele liofilizate sunt încă potrivite pentru consum după mult timp, chiar și fără refrigerare. Termenul „liofilizat” din aceste alimente se referă la procesul de congelare și deshidratarea ulterioară prin sublimarea apei. Pentru ca sublimarea apei să aibă loc, este necesară o combinație de condiții, așa cum se arată în graficul presiune-temperatura, unde liniile reprezintă tranziții de fază.
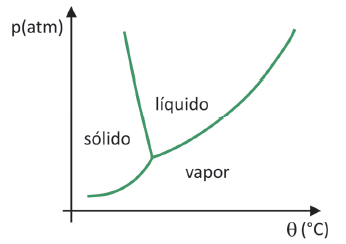
În ciuda faptului că este un proces care necesită, din punct de vedere industrial, utilizarea unei anumite tehnologii, există dovezi că popoarele precolumbienii care locuiau în cele mai înalte regiuni ale Anzilor au putut să liofilizeze alimentele, făcând posibilă păstrarea lor pentru mai mult timp. Verificați alternativa care explică cum a avut loc procesul natural de liofilizare:
a) Sublimarea apei s-a produs datorită temperaturilor scăzute și presiunii atmosferice ridicate din munți.
b) Alimentele, după ce au fost înghețate în mod natural în perioadele reci, erau duse în partea cea mai de jos a munților, unde presiunea atmosferică era mai mică, ceea ce făcea posibilă sublimarea.
c) Mâncarea a fost expusă la soare pentru a crește temperatura, iar presiunea atmosferică locală scăzută a favorizat solidificarea.
d) Temperaturile au fost suficient de scăzute în perioadele reci pentru a îngheța alimentele, iar presiunea atmosferică scăzută din munții înalți a făcut posibilă sublimarea.
e) Alimentele, după ce au fost congelate în mod natural, au fost presate pentru a crește presiunea, astfel încât să se poată produce sublimarea.
Raspuns: litera D.
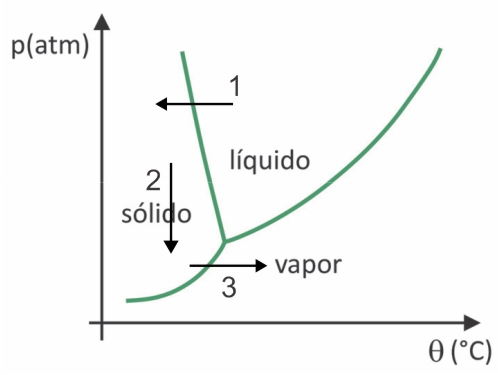
În liofilizare are loc înghețarea apei cu sublimarea ei ulterioară. Popoarele precolumbiene ar putea efectua un astfel de proces, deoarece iarna apa putea îngheța (săgeata 1) și, cu presiunile scăzute (săgeata 2) din cele mai înalte regiuni ale Anzilor, ar putea suferi sublimare (săgeata 3).
intrebarea 2
(Uerj 2005) Gheața carbonică sau dioxidul de carbon solidificat, utilizat pe scară largă în procesele de refrigerare, suferă sublimare în condiții ambientale. În timpul acestei transformări apar, printre altele, fenomenele de variație a energiei și perturbarea interacțiunilor.
Aceste fenomene sunt clasificate, respectiv, astfel:
a) exotermic - interionic
b) exotermic – internuclear
c) izotermic - interatomic
d) endotermic - intermolecular
Raspuns: litera D.
Sublimarea este un proces endotermic, deoarece necesită absorbția de căldură pentru a perturba interacțiunile care mențin moleculele de fază solidă compacte. Aceste interacțiuni sunt de tip intermolecular.
De Stefano Araujo Novais
Profesor de chimie
Aflați mai profund despre acest fenomen.
Răspunsul constă în schimbările de presiune și temperatură.
Aflați despre stările fizice ale materiei și vedeți care sunt acestea. Aflați, de asemenea, ce este Bose-Einstein și unde putem găsi materie în starea de plasmă.
Forțele dipol induse de dipol sunt cele mai slabe forțe intermoleculare care apar între moleculele nepolare.
Vedeți cum să identificați dacă o substanță are un punct de fierbere mai mare decât altul prin relația dintre forțele intermoleculare și punctul de fierbere.