THE baterie este un sistem în care are loc reacția de oxidare-reducere. În acest dispozitiv, energia chimică produsă în reacția spontană este transformată în energie electrică.
Reacțiile de oxidare și reducere apar simultan într-o celulă. Când o specie este supusă oxidării, ea donează electroni celorlalte specii, care, la primirea lor, suferă o reducere.
Prin urmare, cel supus oxidării este agentul reducător, iar cel supus reducerii este agentul de oxidare.
THE oxidare apare atunci când o specie pierde electroni și devine cation: A → A+ + și-.
THE reducere apare atunci când o specie câștigă electroni și devine neutră din punct de vedere electric: B+ + și- → B.
În ecuațiile chimice, aceasta transferul de electroni se demonstrează prin modificarea numărului de oxidare (nox).
Reacțiile de reducere au loc în interiorul celulelor și curentul electric apare odată cu migrarea electronilor de la polul negativ la polul pozitiv.

Cum funcționează o stivă?
unu reactie redox poate fi reprezentat în general prin ecuația:
A + B+ → A+ + B
Unde,
A: substanță care se oxidează, pierde electroni, își mărește valoarea și este agent reducător.
B: substanță care suferă reducerea, câștigă electroni, scade oxidarea și este agentul oxidant.
Vedeți în imaginea următoare cum poate fi reprezentat acest proces.
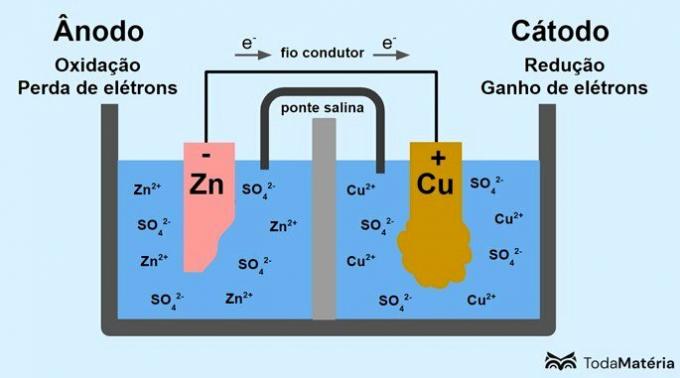
Sistemul împărțit în două semicelule și format din doi electrozi metalici legați extern printr-un fir conductor a fost dezvoltat de John Frederic Daniell (1790-1845) în 1836.
Bateria este formată din doi electrozi, conectați printr-un fir conductor, și un electrolit, unde se află ionii. Electrodul este suprafața solidă conducătoare care permite schimbul de electroni.
anod: electrod la care are loc oxidarea. Este, de asemenea, polul negativ al bateriei.
Catod: electrod la care are loc reducerea. Este, de asemenea, polul pozitiv al bateriei.
În imaginea de mai sus, zincul metalic este anodul și suferă oxidare. Cuprul metalic este catodul și suferă o reducere. Migrarea electronilor (e-) are loc de la anod la catod prin firul conductor.
Reacțiile care apar în sistemul de imagine sunt:
- anod (oxidare): Zn(e) → Zn2(Aici) + 2e-
- Catod (reducere): Cu2+(Aici) + 2e- → fundul(e)
- ecuație generală: Zn(e) + fund2+(Aici) → fundul(e) + Zn2+(Aici)
Zincul este un metal cu o tendință mai mare de a pierde electroni și, prin urmare, în soluție se formează cationi. Electrodul de zinc începe să se uzeze și să piardă din masă deoarece zincul este eliberat în soluție la formarea cationilor de Zn2+.
Electronii din anod ajung la catod iar cationii metalici, la primirea lor, se transforma in cupru metalic, care se depune pe electrod si ii mareste masa.
Puntea de sare este un curent ionic responsabil de circulația ionilor în sistem pentru a-l menține neutru din punct de vedere electric.
Citește și despre numărul de oxidare (nox).
tipuri de baterii
Într-o celulă, tendința speciilor chimice de a primi sau dona electroni este determinată de potențialul de reducere.
Componenta cu cel mai mare potențial de reducere tinde să sufere reducerea, adică să câștige electroni. Speciile cu cel mai mic potenţial de reducere şi, în consecinţă, cu cel mai mare potenţial de oxidare, tinde să transfere electroni.
De exemplu, în reacția redox Zn0(e) + fund2+(Aici) → fundul0(e) + Zn2+(Aici)
Zincul oxidează și donează electroni deoarece are un potențial de reducere E0 = -0,76 V, mai puțin decât potențialul de reducere al cuprului E0 = +0,34V și, prin urmare, primește electroni și suferă o reducere.
Vezi mai jos alte exemple de stive.
Stiva de zinc și hidrogen
Semireacția de oxidare: Zn(e) → Zn2+ + 2e- (ȘI0 = -0,76 V)
Semireacția de reducere: 2H+(Aici) + 2e- → H2 litera (g) (ȘI0 =0,00 V)
Ecuația globală: Zn(e) + 2H+(Aici) → Zn2+(Aici) + H2 litera (g)
Reprezentarea stivei:
Celulă de cupru și hidrogen
Semireacție de oxidare: H2 litera (g) → 2H+(Aici) + 2e- (ȘI0 = 0,00 V)
Semireacția de reducere: Cu2+(Aici) + 2e- → fundul(e) (ȘI0 = +0,34 V)
Ecuația globală: Cu2+(Aici) + H2 litera (g) → 2H+(Aici) + fund(e)
Reprezentarea stivei:
Obține mai multe cunoștințe despre subiect cu conținutul:
- electrochimie
- Electroliză
Referințe bibliografice
FONSECA, M. R. M. Chimie, 2. 1. ed. São Paulo: Attica, 2013.
SANTOS, W.L.P; MOL, G.S. Chimia cetățeană, 3. 2. ed. São Paulo: Editora AJS, 2013.
USBERCO, J. Conectați chimia, 2: chimie. - 2. ed. São Paulo: Saraiva, 2014.


