THE clasificarea periodică a elementelor a fost propusă în 1913 de Henry Monseley (1887-1915), care a identificat variația periodică a multor proprietăţi la intervale regulate în funcţie de numărul de protoni din nucleul atomului unui element chimic.
Din cauza Legea periodicității, criteriul folosit pentru organizarea elementelor Tabelului Periodic actual este ordinea crescătoare a numărului atomic (Z).
Cele 118 elemente chimice sunt aranjate în grupuri și perioade ale Tabelului Periodic. În funcție de proprietățile fizice și chimice, este posibil să se facă distincția între metale, nemetale (nemetale) și semimetale (metaloizi).

Liniile verticale sunt 18 grupuri tabelul și reunesc elemente cu proprietăți chimice similare. Liniile orizontale corespund cu 7 perioade și prezintă elementele cu același număr de straturi electronice.
Hidrogenul este un element care este poziționat deasupra grupului 1 datorită distribuției sale electronice, dar nu are caracteristici comune cu acestea.
Verificați Tabelul periodic completă și actualizată.
metale
Majoritatea elementelor chimice din Tabelul Periodic sunt clasificate ca metale. Principalele caracteristici ale metalelor sunt:
- Au o strălucire caracteristică;
- Sunt dense, maleabile și ductile;
- Sunt buni conductori de electricitate și căldură;
- Sunt prezente în condiții de mediu în stare solidă, cu excepția mercurului.
Elementele metalice ale tabelului periodic sunt:
Metale alcaline (grupa 1): litiu, sodiu, potasiu, rubidiu, cesiu și franciu.
metale alcalino-pământoase (grupa 2): beriliu, magneziu, calciu, stronțiu, bariu și radiu.
Chestiuni reprezentative, pe lângă elementele grupelor 1 și 2, sunt: aluminiu, galiu, indiu, taliu, nion, staniu, plumb, flerovium, bismut, muscovium și livermorium.
Metale de tranziție exterioare sunt elementele care ocupă partea centrală a tabelului periodic:
- Grupa 3: scandiu și ytriu.
- Grupa 4: titan, zirconiu, hafniu și ruterfordiu.
- Grupa 5: vanadiu, niobiu, tantal și dubniu.
- Grupa 6: crom, molibden, wolfram și seaborgiu.
- Grupa 7: mangan, tehnețiu, reniu și bohrium.
- Grupa 8: fier, ruteniu, osmiu și hasiu.
- Grupa 9: cobalt, rodiu, iridiu și meitnerium.
- Grupa 10: nichel, paladiu, platină, darmstadium.
- Grupa 11: cupru, argint, aur și roentgen.
- Grupa 12: zinc, cadmiu, mercur și coperniciu.
Metale de tranziție interne sunt elementele care fac parte din grupa 3 și corespund elementelor seriei lantanide și actinide.
Seria de lantanide este formată din lantan, ceriu, praseodim, neodim, prometiu, samariu, europiu, gadoliniu, terbiu, disproziu, holmiu, erbiu, tuliu, itterbiu și lutețiu.
Seria actinidelor conține elementele actiniu, toriu, protactiniu, uraniu, neptunium, plutoniu, americiu, curiu, berkeliu, californiu, einsteiniu, fermiu, mendeleviu, nobeliu și laurence.
Citiți mai multe despre Metale alcaline.
nemetale
Nemetalele sunt situate în partea dreaptă a tabelului periodic și au caracteristici opuse metalelor, de exemplu:
- Nu au aspect strălucitor;
- Nu sunt buni conductori de electricitate și căldură, deci sunt folosiți ca izolatori;
- Au puncte de fierbere și de topire scăzute, așa că multe se găsesc în natură în stare lichidă.
Tu elemente nemetalice din Tabelul Periodic sunt: hidrogen, azot, oxigen, carbon, fosfor, seleniu, sulf, halogeni și gaze nobile.
Tu halogeni sunt elementele care aparțin grupei 17: fluor, clor, brom, iod, astatin, tenessine și familia gazelor nobile.
Tu gaze nobile sunt elementele care apartin grupei 18: heliu, neon, argon, krypton, xenon, radon, oganesson.
Aflați mai multe despre gaze nobile si halogeni.
semimetale
Semimetale sau metaloizi sunt: bor, siliciu, germaniu, arsen, antimoniu, teluriu și poloniu. Aceste elemente au caracteristici intermediare între metale și nemetale.
Citiți și despre familiile tabelului periodic.
Elemente reprezentative și de tranziție
O altă modalitate de clasificare a elementelor este împărțirea acestora în elemente reprezentative și de tranziție în funcție de distribuția electronică a atomului.
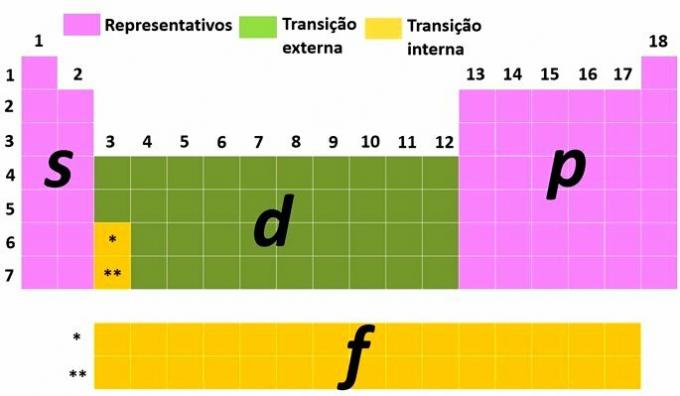
Tu elemente reprezentative sunt cele care au configurația electronică care se termină cu cel mai energetic subnivel în s (grupele 1 și 2) sau pentru (grupele 13, 14, 15, 16, 17 și 18).

Tu elemente de tranziție sunt separate în tranziție externă, cu elementele care au cel mai energetic electron în subnivel d iar cele ale tranziție internă, unde electronul cel mai energetic este într-un subnivel f.

Obține mai multe cunoștințe cu conținutul:
- proprietăți periodice
- Exerciții de tabel periodic
- Exerciții de organizare a tabelului periodic