THE rutherfordiu este un element sintetic cu număr atomic 104, aparținând grupului 4 al Tabelul periodic, fiind primul membru al seriei de transactinide. Prima sa depistare datează din 1964, în celebrele laboratoare ale orașului Dubna. Ca și alte transactinide, numele oficial al elementului 104 a fost implicat într-un conflict între sovietici și americani, într-o piesă din Războiul Rece din istoria chimiei.
rutherfordul nu are aplicatii practice, având în vedere că cel mai stabil izotop al său are aproximativ două ore și jumătate de jumătate de viață. Cu toate acestea, studiile în sisteme și soluții gazoase dovedesc asemănarea chimică cu celelalte elemente din grupa 4, cum ar fi zirconiul și hafniu.
Citeste si: Seaborgium - element sintetic numit după omul de știință Glenn Seaborg
Rezumatul Rutherfordium
- Este un element chimic sintetic situat în grupa 4 din Tabelul Periodic.
- A fost sintetizat pentru prima dată în 1964 la Institutul Comun pentru Cercetări Nucleare din Dubna, Rusia.
- Este un element radioactivbunica.
- Ca și alte transactinide, rutherfordul suferă de stabilitate scăzută și este dificil să sintetizezi probe considerabile pentru studii.
- Numele său a fost oficializat abia în 1997, după câțiva ani de dispute între americani și sovietici.
Proprietățile ruterfordului
- Simbol: Rf
- numar atomic: 104
- masă atomică: 267 c.u.s.
- Configuratie electronica: [Rn] 7s2 5f14 6d2
- cel mai stabil izotop: 267Rf (2,5 ± 1,5 ore timp de înjumătățire)
- serie chimică: grupa 4, transactinide, elemente supergrele
Nu te opri acum... Mai sunt dupa anunt ;)
Caracteristicile Rutherfordium
Ca toate transactinidele, adică elementele imediat după Laurence (Lr), rutherfordium este un element radioactiv. Cel mai stabil izotop al său a fost detectat în 2004 și timpul său de înjumătățire (timpul necesar pentru cantitatea de radioizotop cădere la jumătate) este de două ore și jumătate, cu o marjă de eroare de o oră și jumătate, mai mult sau mai puțin.
Marea dificultate în stabilirea caracteristicilor chimice ale ruterfordiumului și altora transactinide este, în general, faptul că există un ritm scăzut de producție, fie cantitativ, fie în viteză. În aceste elemente, de exemplu, este foarte comun să se evalueze chimic doar unul singur atom, care, într-un fel, necesită adaptări în ceea ce privește calculele, deoarece majoritatea ecuațiilor sunt stabilite pentru sisteme cu mai mult de un atom. În plus, de multe ori izotopii au timpi de înjumătățire foarte scurt, ceea ce face ca studiile mai aprofundate să fie dificile sau chiar imposibile.
În cazul specific al Rf, oamenii de știință au reușit deja să demonstreze că comportamentul său în fază lichidă este similar cu cel al altor elemente. mai usor grupa 4, zirconiu si hafniu, ca la formarea fluorurilor in solutie cu extragere ulterioara in rasini schimbătoare de ioni. Acest comportament a ajutat la solidificarea prezenței ruterfordului în grupa 4 din Tabelul Periodic.
Citeste si tu: Elemente chimice noi — cele patru elemente lipsă în perioada a 7-a
Obținerea Rutherfordium
Transactinidele au nevoie de o infrastructură mare pentru producția lor. Toate sunt sintetizate cu acceleratori de particule, în care speciile ionice se ciocnesc cu elemente grele. De asemenea, detectarea acestor elemente nu este simplă și directă.
Când se formează, elementul radioactiv, prin natura sa, începe să se descompună și să prezinte emisii, cum ar fi particulele alfa și beta. Este adesea necesar să se evalueze dezintegrare radioactivă a atomului format sau chiar identificați speciile atomice care pot apărea din aceste reacții nucleare, ca într-un puzzle.
Adăugați asta la faptul că timpul de înjumătățire al izotopilor transactinide este adesea scurt, în intervalul de secunde, făcând posibilă obținerea doar a unei cantități în intervalul câțiva atomi sau chiar a unui singur atom.
În cazul Rf, prima sinteză raportată pentru acest element a implicat ciocnirea izotopilor de plutoniu, Pu, cu ionii izotopului de neon 22, huh.
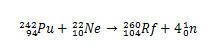
Cu toate acestea, alți izotopi ai ruterfordiumului pot fi produși prin modificarea speciilor care se vor ciocni. De exemplu, izotopul 261 poate fi produs prin reacția dintre oxigen-18 și curiu-248, producând cinci neutroni.
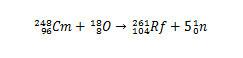
Consultați-l pe podcastul nostru: Cum funcționează un accelerator de particule?
Precauții cu Rutherfordium
Deoarece ruterfordul nici măcar nu poate fi produs la o scară considerabilă, riscurile asociate cu acest element sunt legate de efecte ale radiatii. Cu toate acestea, într-un laborator controlat, aceste riscuri sunt anticipate și astfel minimizate.
Istoria Rutherfordiului

Toate transactinidele au fost implicate într-o cursă pentru descoperirea lor în anii 1960 și 1970. Acest episod este raportat ca Războiul transferurilor, o parte din Război rece în istoria chimiei. În ciuda faptului că este numit așa, ceea ce sugerează că disputele au avut loc asupra elementelor după fermiu, un element numărul atomic 100, elementele direct implicate erau de la 104 la 109, noul descoperit transactinide.
În cazul rutherfordiului, disputa a început în 1964., când cercetătorii sovietici de la Institutul Comun pentru Cercetări Nucleare din orașul Dubna Rusia, a raportat descoperirea elementului 104 izotop 260 prin bombardarea plutoniului-242 cu ioni neon-22. Dar cercetătorii Dubna au prezentat doar o singură dovadă, care a fost detectarea unui izotop care s-a degradat spontan, fără a-i identifica clar masa și timpul de jumătate de viață. Drept urmare, descoperirea a fost privită cu suspiciune.
Cinci ani mai târziu, în 1969, o echipă de oameni de știință americani de la Laboratorul Național Lawrence Berkeley din Berkeley, California, condusă de Albert Ghiorso, a spus că a oferit suficiente dovezi pentru descoperirea izotopului 257 elementului 104 prin ciocnirea californiului-249 cu carbon-12. Aceiași oameni de știință au reușit ulterior să producă izotopul 259 al elementului 104. În 1973, oamenii de știință de la Laboratorul Național Oak Ridge au confirmat în mod independent numar atomic 104 pentru izotopul de masă 257 produs la Berkeley.
Anii următori au fost de mare dispută între oamenii de știință din cele două țări, până când, în 1985, de Chimie Pură și Aplicată (IUPAC) și Uniunea Internațională de Fizică Pură și Aplicată (IUAP) forma a comisie mixtă de nouă oameni de știință, numită Grupul de lucru pentru transferuri (Grupul de lucru Transferium sau TWG). TWG a fost creat pentru a decide cine a fost de fapt responsabil pentru descoperirile elementelor cuprinse între 101 și 112.
Chiar și așa, deciziile TWG nu au fost întotdeauna fără îndoială. În cazul elementului 104, grupul de lucru a decis că Creditul ar trebui împărțit între oamenii de știință sovietici și americani, ceva ce oamenilor de știință din Berkeley nu le-a plăcut deloc.
În 1991, Ghiorso și Seaborg, din echipa Berkeley, au susținut chiar că identificarea elementului 104 de către oamenii de știință de la Dubna a fost în mod clar greșit și, la un moment dat, a negat validitatea concluziilor TWG, considerându-le un deserviciu comunității. științific.
Nu e de mirare, în La începutul anilor 1990, numele noilor elemente nu erau încă un consens.. Au fost apoi negocieri în care au fost implicați oameni de știință germani, ruși și americani, care s-au dovedit a fi frustrate. Acolo, în 1992, laboratorul german Gesellschaft für Schwerionenforschung (GSI) a propus nume pentru elementele de la 102 la 109, punând meitnerium pentru elementul 104.
Chiar și așa, lista, deși lăudată, nu a fost acceptată de oamenii de știință implicați. Decizia ar putea fi luată în 1994, în cadrul conferinței Comisiei de nomenclatură a compușilor anorganici (CNIC) Iupac. În ea, numele dubnium a fost ales pentru elementul 104, cu toate acestea, Societatea Americană de Chimie a adoptat, în același an, denumirea de rutherfordium pentru elementul 104. elementul 104, într-un moment de discredit din partea americanilor, care au ajuns să pună la îndoială autoritatea IUPAC de a oficializa noi nume.
abia în 1997, la conferința generală IUPAC de la Geneva, este asta elementul 104 a fost în cele din urmă oficializat ca rutherfordium, după ce ACS a cedat în nomenclatorul altor elemente din apropiere.
Exerciții rezolvate pe rutherfordium
intrebarea 1
Rutherfordul este un element sintetic și una dintre principalele dificultăți în studierea lui este faptul că nu este posibil să sintetizeze cantități mari din acesta.
Dintre posibilii factori care contribuie la aceasta dificultate, putem indica:
(A) Rutherfordium are izotopi cu timp de înjumătățire lung de ordinul milioanelor de ani.
(B) Rutherfordium se descompune spontan și foarte rapid, împiedicând detectarea cantităților sale macroscopice.
(C) Nu există tehnologii capabile să sintetizeze ruterfordul, datele lor fiind strict teoretice și fără bază științifică.
(D) Legile chimiei afirmă că este imposibil să sintetizezi elemente al căror număr atomic îl depășește pe cel al lui Lawrence, 103.
(E) În timpul sintezei ruterfordului, elementele mai ușoare din grupul său sunt prioritizate din punct de vedere chimic.
Răspuns: litera B
Elementele transactinide, cum ar fi Rf, sunt radioactive și se descompun spontan la viteză mare, deoarece timpul lor de înjumătățire este scurt. Astfel, la sfârșitul experimentului, din specia sintetică au mai rămas puțini atomi.
intrebarea 2
În 1964, cercetătorii de la Dubna au susținut că au sintetizat izotopul ruterfordiu-260 (Z = 104). În cazul acestui izotop, care este numărul de neutroni?
(A) 104
(B) 260
(C) 151
(D) 156
(E) 161
Răspuns: litera D
Numarul neutroni (n) se poate calcula, folosind numărul de masă (A) și numărul atomic (Z), prin următoarea ecuație:
A = Z + n
Înlocuind, avem:
260 = 104 + n
n = 260 - 104
n = 156
credite de imagine
[1] abas trandafir / oblon
De Stefano Araújo Novais
Profesor de chimie


