Electroliză este un proces non-spontan, adică unul care nu are loc în mod natural, în care substanțele se formează prin intermediul unei descărcări electrice în compuși topiți sau dizolvați în apă. În acest proces, un curent electric ajunge într-un recipient de sticlă (rezervor electrolitic) care are doi electrozi inerti (care nu suferă sau oxidare nici reducere) format din grafit sau platină. Acești electrozi sunt conectați la o sursă electrică (de obicei a tobe) și înmuiat într-o sare sau bază topită sau dizolvată în apă. La fel ca baterie, electroliza are un catod (unde are loc reducerea) și un anod (unde are loc oxidarea).
rezumat
Electroliza este un proces non-spontan;
Se pot forma substanțe simple sau compozite;
Poate să apară cu un dizolvat topit (electroliză magmatică);
Poate apărea cu un dizolvat dizolvat în apă (electroliză apoasă);
Un cation suferă întotdeauna reducere la catod;
Un anion suferă întotdeauna oxidare la anod.
Vezi și:Obținerea aluminiului din electroliză

Tipuri de electroliză
Este o electroliză care are loc atunci când se efectuează o descărcare electrică asupra unui compus ionic topit. Compusul ionic este unul format dintr-o legătură ionică, cum ar fi a sare sau a baza anorganic. Când vorbim despre compus topit, la rândul nostru, ne referim la compusul care trece de la o stare solidă la una lichidă.
- Exemplu de electroliză magmatică
Când efectuăm fuziunea clorurii de potasiu (KCl), această sare este supusă procesului de disociere, eliberând cationul de potasiu (K+) și anionul de iodură (l-).

Ecuația de disociere pentru clorura de potasiu
Când curentul electric ajunge la celula electrolitică cu acești ioni, cationul de potasiu este redus, formând potasiu metalic (K), iar anionul de iod este oxidat, formând iod solid (I2).
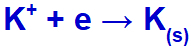
Ecuația formării de potasiu solid
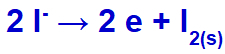
Ecuația de formare a iodului solid
Este o electroliză care are loc atunci când descărcarea electrică este efectuată pe o soluție apoasă (are apă) formată dintr-o sare sau o bază anorganică.
- Exemplu de electroliză apoasă
Când dizolvăm clorura de sodiu în apă, aceasta se disociază, iar apa suferă ionizare:

Ecuații de ionizare a apei și de disociere a clorurii de sodiu
Ca cation de sodiu (Na+) aparține familiei IA, cationul de hidroniu (H+) trece prin descărcare și suferă reducere, formând hidrogen gazos (H2).
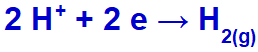
Ecuația formării gazului hidrogen
Ca clorură (Cl-) nu este oxigenat (nu are oxigen) și nu este fluor (F-), este evacuat, oxidându-se și formând clor gazos (Cl2).

Ecuația formării gazului clor
Descărcare ionică selectivă
În timpul unui proces de electroliză într-un mediu apos (soluție formată din apă și solut), vom avea întotdeauna doi cationi: hidroniu, din apă și oricare altul, din disocierea sării (un exemplu de solut). Vom avea, de asemenea, doi anioni: hidroxilul, care provine din apă, și altul, care provine din sare.

Ionii din ionizarea apei și disocierea sării
- Descărcare selectivă pentru cationi și anioni
Dacă cationul din soluție aparține familiei IA, IIA sau IIIA, hidroniul (H+) va fi redus;
Dacă cationul care provine din solut nu aparține familiilor menționate mai sus, va suferi reducerea.
Dacă anionul din soluție are oxigen în compoziția sa sau este fluor (F-), hidroxidul (OH-) va suferi oxidare;
Dacă anionul din solut nu are caracteristicile de mai sus, va suferi oxidare.
Se știe că apa are capacitatea de auto-ionizare, producând ioni de hidroniu (H+) și hidroxid (OH-), dar această ionizare este destul de limitată. Acest fapt este dovedit de ineficiența apei pure în conducerea curentului electric.
Ca electroliză implică descărcare electrică, pentru a efectua electroliza apei, este necesar să se dizolve un solut, care favorizează descărcarea selectivă a hidroniului și a hidroxidului (așa cum se vede în subiectul privind descărcarea selectiv).
Dacă adăugăm sulfat de sodiu (Na2NUMAI4), de exemplu, vom avea cationii de sodiu la mijloc (Na+) și hidroniu (H+), precum și anioni hidroxid (OH-) și sulfat (SO4-2). Astfel, când curentul electric ajunge în rezervorul electrolitic:
hidroniul va fi descărcat, reducând, deoarece sodiul aparține familiei IA;
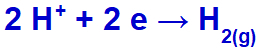
Ecuația formării gazului hidrogen
hidroxidul se va descărca, oxidându-se, deoarece sulfatul are oxigen în compoziția sa.
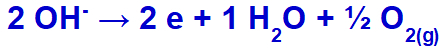
Ecuația formării gazului de oxigen
Întrucât cei doi ioni (cation și anion) care provin din apă au fost descărcați, spunem că electroliza apei a avut loc.
Vezi și tu: Aspecte cantitative ale electrolizei
Producerea de substanțe simple precum hidrogen gazos (H2), oxigen gazos (O2) etc .;
Producerea de substanțe compozite precum hidroxid de sodiu (NaOH), acid sulfuric (H2NUMAI4) etc;
Acoperirea unei piese cu un anumit metal, cum ar fi cuprul (cupru) și aurul (placare cu aur);
Folosiți pentru a îndepărta un anumit metal din minereu.
Exerciții rezolvate de electroliză
Exemplul 1 - (Vunesp) O soluție apoasă de CuCℓ2 este supus electrolizei, folosind electrozi de platină. Afirmația corectă este:
a) Reducerea ionului cu are loc la catod2+.
b) Oxidarea ionilor de cu are loc la anod2+.
c) La catod se formează clor gazos.
d) O parte din anodul de platină se dizolvă, formând Pt2+.
e) Produsele acestei electrolize ar fi diferite dacă electroliza CuCl2 a fost aprins (fuziune).
a) Corect. Când CuCl2 este dizolvat în apă, avem cationii de hidroniu (H+) și cupru II (Cu+2). Deoarece cationul cupru II nu aparține familiilor IA, IIA și IIIA, este redus.
b) Fals, deoarece anionul clorură (Cl) este oxidat la anod-), care nu are oxigen în compoziția sa și nu este fluor (F-).
c) Fals, deoarece reducerea cationului de cupru II are loc la catod, prin urmare, există formarea metalului de cupru.
d) Fals, deoarece electrozii de platină sau grafit în electroliză conduc doar electricitatea, nu participă la proces.
e) Fals, ca electroliză ígnea a clorurii de cupru II (CuCl2) ar prezenta exact aceleași produse ca și cele apoase, deoarece ionii prezenți ar fi cuprul II (Cu+2) și clorura (Cl-1).
Exemplul 2- (UFRN) Luați în considerare următoarele sisteme:
I. Clorură de sodiu topită;
II. Soluție apoasă de clorură de sodiu;
III. Hidroxid de sodiu condensat;
IV. Soluție apoasă de hidroxid de sodiu.
Cei care pot furniza sodiu, atunci când sunt supuși electrolizei, sunt:
a) numai eu și II.
b) numai I și III.
c) numai II și IV.
d) numai III și IV.
e) I, II, III și IV.
Sistemele care furnizează sodiu metalic ca produs la catod sunt I și III.
I- Singurul cation prezent în mediu este cationul de sodiu, prin urmare, numai acesta se poate reduce, formând sodiu metalic.
II- Acest sistem nu prevede sodiu metalic deoarece clorura de sodiu a fost dizolvată în apă, prin urmare, la mijloc avem prezența cationilor de sodiu (Na+) și hidroniu (H+) - acesta este cel care suferă reducerea, deoarece sodiul aparține familiei IA.
III- Singurul cation prezent în mediu este cationul de sodiu (deoarece materialul a fost supus unei fuziuni), prin urmare, numai acesta suferă o reducere, formând sodiu metalic;
IV- Acest sistem nu oferă sodiu metalic deoarece hidroxidul de sodiu a fost dizolvat în apă, deci la mijloc avem prezența cationilor de sodiu (Na+) și hidroniu (H+) - acesta este cel care suferă reducerea, deoarece sodiul aparține familiei IA.
De mine. Diogo Lopes Dias