La reacţii de oxidare cu alcooli secundari sunt cele în care interacţiunea dintre un compus organic din grupul de alcooli, care trebuie să fie secundar, și așa-numitul reactiv Bayer (KMnO4) într-un mediu acid.
Ori de câte ori reactivul Bayer este într-un mediu acid (aq/H+), suferă o reacție de descompunere, dând naștere oxidului de potasiu, oxidului de mangan II și oxigenului în curs de dezvoltare, după cum se poate observa în următoarea ecuație:
2 kmnO4(aq/H+) → 2 MnO + K2O + 5 [O]
În orice reacție de oxidare, oxigenii în curs de dezvoltare, provenit din descompunerea permanganatului de potasiu într-un mediu acid, ataca lanțurile de carbon care au legături pi între atomi de carbon (alchene, alchine și alcadiene) sau care sunt închise (ciclani, cicluri aromatici), generând noi compuși chimici.
În cazul în care reacție de oxidare în alcooli secundari, înainte de a înțelege mecanismul de reacție, este necesar să ne amintim conceptul de alcool secundar. se numește alcool secundar unul în care hidroxilul (OH) este legat de a
carbon secundar (carbon legat direct de alți doi atomi de carbon). Vezi reprezentarea unui alcool secundar: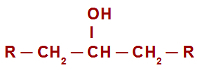
Formula generală de structură a unui alcool secundar
În fiecare reacție de oxidare în alcooli, oxigenii în curs de dezvoltare atacă hidrogenii aflați pe carbonul care are grupa hidroxil. În cazul reacțiilor de oxidare în alcoolii secundari, oxigenii au doar un atom de hidrogen de atacat în fiecare structură a acestui tip de alcool.
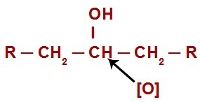
Oxigenul nascut ataca un alcool secundar
Când atacă hidrogenul (H) prezent în carbonul hidroxil (OH), oxigenul în curs de dezvoltare ([O]) formează un nou hidroxil pe acelasi carbon. Deci avem un gemino diol în închisoare. Deoarece geminodiolul (HO – C – OH) este instabil, se descompune într-o moleculă de apă.Cu toate acestea, între carbonul și oxigenul rămas de la unul dintre hidroxili, are loc formarea unei duble legături (pi și sigma).
Nu te opri acum... Mai sunt dupa publicitate ;)
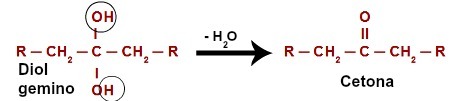
Ecuația chimică a oxidării unui alcool secundar
Produsul care provine dintr-o reacție de oxidare a alcoolilor secundari este întotdeauna a cetonă, căci dubla legătură se generează întotdeauna la carbonul secundar, ceea ce are ca rezultat un carbonil între doi atomi de carbon, formând astfel o cetonă.
Vezi acum a exemplu de reacție de oxidare în alcooli secundari.
Exemplu: Butan-2-ol
O butan-2-ol este un alcool secundar, deoarece hidroxilul este atașat la un atom de carbon secundar. Deci, pe carbonul care are hidroxilul, există un singur hidrogen. Putem verifica acest fapt în structura de mai jos:

Când este supus unui mediu care conține apă, acid și KMnO4 (reactivul Bayer), the hidrogenul tău este atacat de un oxigen în curs de dezvoltare, transformându-se într-un nou hidroxil, care are ca rezultat un geminodiol.

În cele din urmă, există o descompunere a celor doi hidroxili prezenți în geminodiol, rezultând astfel o moleculă de apă și o cetonă, datorită necesității de a crea o legătură între carbon și unul dintre oxigenii hidroxililor descompusi.

putem reprezenta întreaga reacție de oxidare a butan-2-olului prin următoarea ecuație:

De mine. Diogo Lopes Dias
Doriți să faceți referire la acest text într-o lucrare școlară sau academică? Uite:
ZILE, Diogo Lopes. „Reacții de oxidare în alcooli secundari”; Scoala din Brazilia. Disponibil in: https://brasilescola.uol.com.br/quimica/reacoes-oxidacao-alcoois-secundarios.htm. Accesat pe 27 iulie 2021.
Chimie

Grupa funcțională hidroxil, alcooli primari, alcooli secundari, alcooli terțiari, metanol, glicerol, etanol, prepararea nitroglicerinei, fabricarea vopselei, producția de băuturi alcoolice, acid acetic, combustibil automobile.