Polimerizare este denumirea procesului chimic care are ca rezultat formarea de macromolecule (molecule mari) numite polimeri, prin combinarea unor molecule mai mici, monomerii.
reactia lui polimerizare este foarte frecventă în natură, așa cum putem vedea în carbohidrați (cum ar fi amidonul) și proteine (cum ar fi cazeina din lapte). Apare și pe cale sintetică, deoarece marea majoritate a polimerilor folosiți de ființele umane în viața lor de zi cu zi sunt fabricați artificial.
Primul polimer produs din polimerizare sintetic a fost bachelita, în 1909, de chimistul belgian Leo Hendrik Baekeland.
În general, pentru ca un monomer să fie combinat cu altul (fie că sunt la fel sau diferiți) într-o reacție de polimerizare, este necesară existența valenței libere (legătura chimică de realizat) în ambii monomeri.
Aceste valențe apar ca urmare a ruperii legăturilor, prin utilizarea catalizatorilor (cum ar fi nichelul), condiții externe precum lumina și căldura, sau prin fenomenul de rezonanță în structură (deplasarea electronilor).
În formarea polipropilenei (polimer PP), de exemplu, utilizată în ustensile de uz casnic și jucării, pi link (π) în fiecare moleculă este defalcat după cum urmează:
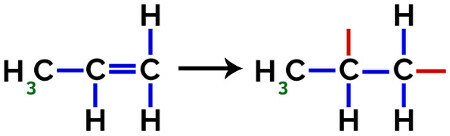
Ruperea legăturii pi în propilenă
Astfel, fiecare monomer de propilenă se poate lega cu alți doi monomeri de propilenă și poate forma polimerul PP sau polipropilenă (prefixul poli indică mai multe unități monomerice). Cea mai frecventă modalitate de a reprezenta un polimer o are monomerul între paranteze și, în exterior, litera n, care indică mai mulți monomeri, așa cum putem observa în cazul polimerului PP:
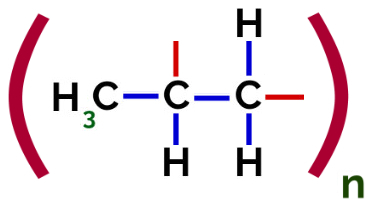
Reprezentarea polimerului PP
reactia lui polimerizare se poate face în diferite moduri, după cum vom vedea mai jos:
a) Reacția lui polimerizare prin adiție
In acest polimerizare, există întotdeauna o rupere a unei legături pi în monomer, ceea ce face ca în structură să apară două valențe libere, ca în formarea polietilenă, polimer utilizat pe scară largă în ambalajele farmaceutice.
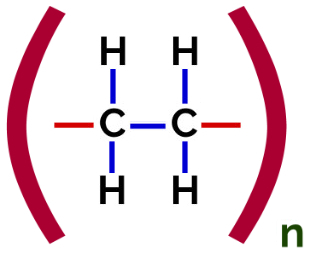
Polietilenă de adaos Polimer Formula structurală
La polimerizare de polietilenă, ca monomer se folosesc molecule de etilenă (etenă), care au o legătură pi între cei doi atomi de carbon. Când această legătură este ruptă, apar două valențe libere, câte una pe fiecare atom de carbon care a fost implicat în legătura pi. Monomerii se unesc exact în fiecare dintre aceste valențe, adică valența unuia este legată de valența celuilalt și așa mai departe.
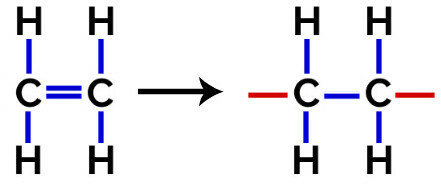
Ecuația formării polietilenei
b) Reacția de polimerizare prin adiție 1.4
În această polimerizare, monomerii prezintă două legături duble alternative (una pi și una sigma), ceea ce favorizează fenomenul de rezonanță (alternarea poziției electronilor pi ai legăturii pi), ca în formarea cauciucului sintetic (polibutadienă)

Formula structurală a polibutadienei
Unitatea monomerică a acestui polimer este butadiena, care are două legături duble alternative. Cu rezonanță, structura are o legătură dublă între atomii 2 și 3 și două valențe libere pe atomii 1 și 4. Tocmai în aceste valențe libere ale atomiilor 1 și 4 se combină monomerii.

Rezonanță butadienă
c) Reacția lui polimerizare prin condensare sau eliminare
Este o reacție a polimerizare în care, în mod obligatoriu, doi monomeri (aceeași sau diferiți) pierd simultan atomi sau grupări, rezultând două valențe libere în fiecare dintre ei. În acest fel, există întotdeauna eliminarea hidrogenului dintr-un monomer, care apoi se unește cu un halogen (F, Cl, Br, I), OH, NH2, sau la CN al celuilalt monomer.
Deci, în polimerizare prin eliminare, se formează întotdeauna apă, acid halogenat (HCl, HI, HF, HBr), amoniac (NH3) sau acid cianhidric (HCN) în plus față de polimer. A se vedea, de exemplu, reprezentarea formării poliesterului, un material folosit ca țesătură:

Ecuația formării poliesterului
Monomerii care formează poliester sunt acidul p-benzendioic și etan-1,2-diol. Putem observa că în aceasta polimerizare are loc eliminarea moleculelor de apă, deoarece cei doi monomeri au doi hidroxili. În acest proces, acidul pierde cei doi hidroxili, iar dialcoolul pierde doar hidrogenul din hidroxilii săi:

Structură din poliester
Monomerii poliesterici sunt uniți de oxigenul din alcool și carbonul din acidul carboxil.
De mine. Diogo Lopes Dias
Sursă: Brazilia școală - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm
