Kp este acronimul folosit pentru a determina constanta unui echilibru în ceea ce priveşte presiunile parţiale. Această constantă funcționează cu valorile participanților gazoși ai unui echilibru în unitatea atm, de exemplu.

Ecuația reprezentând o reacție chimică cu componente gazoase
În această ecuație, toți participanții sunt gazoși, deci atunci când un gaz participant are a presiune parțială în amestec, este reprezentat de abrevierea pX.
La stabilirea ecuației de echilibru chimic (din punct de vedere al concentrației), produsele trebuie plasate la numărător, iar reactanții sunt plasați la numitor:
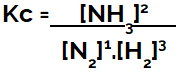
Expresia Kc a echilibrului de formare a amoniacului
expresia lui constanta de echilibru in termeni de presiune (Kp) urmează tiparul de Kc, adică presiunile parțiale ale reactivilor sunt poziționate la numitor și presiunile parțiale ale produselor la numărător:
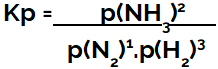
Expresia Kp a echilibrului de formare a amoniacului
Observare: Dacă ecuația de reacție a lui echilibru chimic nu prezentați niciun participant gazos, acesta nu se va prezenta automat Kp.
Exemplu: (PUC-MG) Pentru reacție: 2 CO(g) + O2 litera (g)? 2 CO2 litera (g), presiunile parțiale ale CO(g) este2 litera (g) la echilibru ele sunt, respectiv, 0,2 atm, respectiv 0,4 atm. Presiunea totală a sistemului este de 1,4 atm. Valoarea a Kp pentru că reacția este:
a) 56.2
b) 40,0
c) 35,6
d) 28.4
e) 25,6
Datele furnizate de exercițiu sunt:
Presiunea parțială a monoxidului de carbon (pCO) = 0,2 atm;
Presiunea parțială a monoxidului de carbon (pO2) = 0,4 atm;
Presiune totală =1,4 atm;
Pentru a determina Kp al acestui sistem, trebuie să parcurgem următorii pași:
Pasul 1: Determinați presiunea parțială a monoxidului de carbon (pCO2).
Pentru aceasta, amintiți-vă că presiunea totală (pt) este suma tuturor presiunilor parțiale:
pt = pCO + pCO2 + pO2
1,4 = 0,2 + p (CO2) + 0,4
1,4 - 0,2 - 0,4 = pCO2
pCO2 = 0,8 atm
Pasul 2: Determinați Kp al exercițiului.
Pentru aceasta, utilizați doar valorile în expresia constantei de echilibru Kp:
Kp = (pCO2)2
(pCO)2.(praf2)1
Kp = (0,8)2
(0,2)2.(0,4)1
Kp = 0,64
0,04.0,4
Kp = 0,64
0,016
Kp = 40 atm-1
De mine. Diogo Lopes Dias
Sursă: Brazilia școală - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kp.htm

