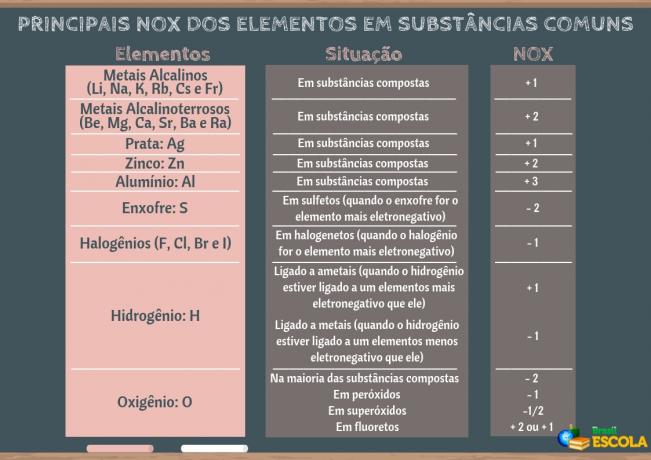
PH-ul corespunde potențialului hidrogen al unei soluții. Este determinată de concentrația ionilor de hidrogen (H+) și servește la măsurarea gradului de aciditate, neutralitate sau alcalinitate a unei soluții date.
În plus față de pH, există și o altă cantitate care determină aciditatea și bazicitatea unui sistem apos: pOH (potențial hidroxilionic). Această scală are aceeași funcție ca pH-ul, deși este mai puțin utilizată.
scara pH-ului
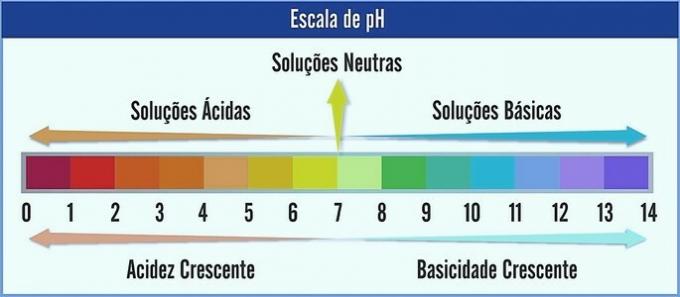
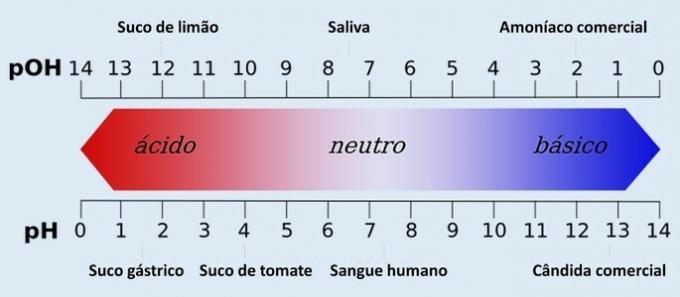
PH-ul este reprezentat pe o scară cuprinsă între 0 și 14. Măsoară aciditatea și basicitatea unei soluții.
Prin urmare, pH 7 reprezintă o soluție neutră (de exemplu, apă pură). Cele dinaintea acestuia sunt considerate soluții acide (pH acid), iar cele după 7 sunt soluțiile bazice (pH alcalin).
Cu această observație făcută, caracterul acid crește de la dreapta la stânga. Personajul de bază, de la stânga la dreapta. Rețineți că cu cât valoarea pH-ului este mai mică, cu atât soluția va fi mai acidă.
Aflați mai multe la:
- Soluție tampon
- Titrare
- Reacție de neutralizare
Exemple
Soluții acide
| Soluţie | pH |
|---|---|
| Suc gastric | 2,0 |
| Suc de lămâie | 2,2 |
| Oţet | 3,0 |
| Cafea | 5,0 |
| Lapte de vaca | 6,4 |
Soluții de bază
| Soluţie | pH |
|---|---|
| sânge uman | 7,35 |
| Apa de mare | 7,4 |
| Bicarbonat de sodiu | 8,4 |
| Lapte de magnezie | 10,5 |
| Albire | 12,5 |
Cum se calculează pH-ul?
În 1909, chimistul danez Soren Sörensen (1868-1939) a propus ca aciditatea soluțiilor, măsurată în concentrații de ioni H+, valorile sale au fost transformate folosind logaritmi pentru a facilita înțelegerea.
La o temperatură de 25 ° C, produsul ionic al apei este egal cu 10–14 mol2/ L2.
Aplicând cologaritmul în expresie, trebuie să:
Prin această expresie, putem obține valoarea corespunzătoare de la o scară la alta prin scădere.
Cum se măsoară pH-ul?
Controlul pH-ului este important nu numai în scopuri științifice, ci și în viața de zi cu zi.
PH-ul bazinului trebuie verificat, precum și pH-ul acvariului și chiar pH-ul solului pentru a permite anumite tipuri de culturi.
Mai jos sunt principalele modalități de măsurare a pH-ului.
indicator acid-bazic
Așa-numiții indicatori acid-bazici sunt utilizați pentru a măsura pH-ul unei soluții. Sunt substanțe care își schimbă culoarea, indicând caracterul soluției. Cei mai utilizați indicatori sunt: turnesol și fenolftaleină.

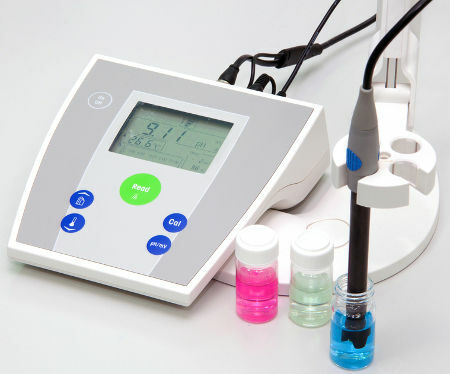
Pedometru
În plus față de indicatori, pH-ul unei soluții poate fi măsurat folosind un instrument numit peagometru. Acest dispozitiv electronic măsoară conductivitatea electrică a soluției și o convertește la scara valorilor pH-ului.

Exerciții de examen de admitere cu feedback
1. (Enem / 2014) Un cercetător realizează că eticheta unuia dintre paharele în care păstrează un concentrat de enzime digestive este ilizibilă. Nu știe ce enzimă conține paharul, dar suspectează că este o protează gastrică, care funcționează în stomac prin digestia proteinelor.
Știind că digestia în stomac este acidă și intestinul este de bază, el asamblează cinci eprubete cu alimente diferit, adăugați concentratul enzimatic la soluțiile cu un pH determinat și așteptați să vedeți dacă enzima acționează în vreunul al lor.
Eprubeta în care enzima trebuie să acționeze pentru a indica faptul că ipoteza cercetătorului este corectă este cea care conține:
a) cub de cartofi în soluție cu pH = 9
b) bucată de carne în soluție cu pH = 5
c) albuș de ou fiert în soluție cu pH = 9
d) porție de tăiței în soluție cu pH = 5
e) bilă de unt în soluție cu pH = 9
Alternativă corectă: b) bucată de carne în soluție cu pH = 5.
Protează este o enzimă care digeră proteinele și, deoarece este gastrică, acționează în stomac, al cărui pH este acid.
Analizând alternativele, trebuie să:
a) GRESIT. Cartofii au un conținut ridicat de carbohidrați, iar pH-ul concentratului este de bază.
b) CORECT. Carnea conține proteine și enzimele pot acționa asupra ei, iar pH-ul concentratului este acid, la fel ca stomacul.
c) GRESIT. PH-ul concentratului este de bază.
d) GRESIT. Pastele sunt bogate în carbohidrați.
e) GRESIT. PH-ul concentratului este de bază.
2. (Udesc / 2009) „Ploaia acidă” este un termen care se referă la precipitațiile din atmosfera ploii cu cantități mai mari decât cele normale de acizi azotici și sulfurici.
Precursorii ploii acide provin atât din surse naturale, cum ar fi vulcanii și vegetația în descompunere, cât și din procese emisiile industriale, în principal dioxidul de sulf și oxizii de azot din combustibilii arși fosile.
PH-ul apei de ploaie considerat normal este de 5,5 (datorită prezenței acidului carbonic din solubilizarea dioxidului de carbon). Un chimist care monitoriza o regiune extrem de industrializată a observat că pH-ul apei de ploaie a fost de 4,5.
Având în vedere că aciditatea este legată de concentrația de H3O+, este corect să spunem că apa cu pH 4,5 a fost:
a) de două ori mai simplu decât cel normal.
b) de două ori mai acid decât în mod normal.
c) de zece ori mai de bază decât în mod normal.
d) de zece ori mai acid decât normal.
e) de o sută de ori mai acidă decât în mod normal.
Alternativă corectă: d) de zece ori mai acidă decât în mod normal.
Conform expresiilor pH = - log [H+] si H+] = 10-pH, Noi trebuie sa:
pH = 5,5
[H+] = 10-5,5
pH = 4,5
[H+] = 10-4,5
Diferența dintre valori este: 10- 5,5 - ( - 4,5) = 10 -1
Deoarece scara pH-ului este o scară logaritmică, schimbarea unei unități este egală cu o soluție de 10 ori mai acidă.
3. (UFMG / 2009) Luați în considerare o anumită cantitate de apă și suc de lămâie, amestecate, conținute într-un pahar. Consultați aceste trei afirmații referitoare la acest sistem:
I. Sistemul este acid.
II. PH-ul sistemului este mai mare de 7.
III. În sistem, concentrația ionilor H+ este mai mare decât OH–.
Pe baza acestei analize, este CORECT să afirmăm că:
a) numai afirmațiile I și II sunt corecte.
b) numai afirmațiile I și III sunt corecte.
c) numai afirmațiile II și III sunt corecte.
d) toate cele trei afirmații sunt corecte.
Alternativă corectă: b) numai afirmațiile I și III sunt corecte.
I. CORECT Lămâia conține acid citric, care în soluție eliberează ioni H+ și astfel sistemul este acid.
II. GRESIT. PH-ul este mai mic de 7, caracterizând un sistem acid: cu cât pH-ul soluției este mai aproape de 0, cu atât este mai acid.
III. CORECT PH-ul acid este rezultatul concentrației ridicate de ioni H+ în soluție, deoarece pH = - log [H+].
Pentru mai multe întrebări, cu rezoluție comentată, asigurați-vă că verificați:Exerciții de pH și pOH.