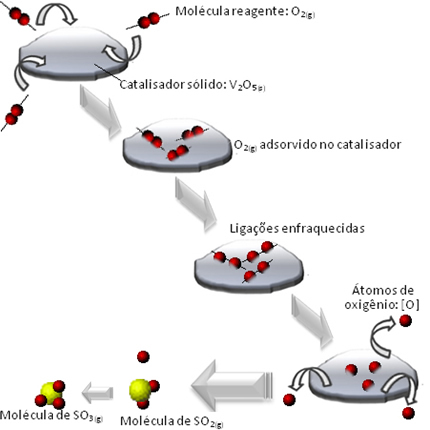
Chimistul francez Henri Louis Le Chatelier a creat una dintre cele mai cunoscute legi ale chimiei care prezice răspunsul sistemului chimic în echilibru atunci când este expus la o modificare.
Cu rezultatele studiilor sale, el a formulat o generalizare pentru echilibrul chimic care afirmă următoarele:
„Când un factor extern acționează asupra unui sistem în echilibru, acesta se mișcă, întotdeauna în sensul de a minimiza acțiunea factorului aplicat.”
Atunci când echilibrul unui sistem chimic este perturbat, sistemul acționează pentru a minimiza această perturbare și a restabili stabilitatea.
Prin urmare, sistemul prezintă:
- o stare inițială de echilibru.
- o stare „dezechilibrată” cu schimbarea unui factor.
- o nouă stare de echilibru care se opune schimbării.
Exemple de tulburări externe care pot afecta echilibrul chimic sunt:
| Factor | Tulburări | Este făcut |
|---|---|---|
| Concentraţie | Crește | Consumați substanța |
| Scădea | substanța este produsă | |
| Presiune | Crește | Se deplasează la cel mai mic volum |
| Scădea | Se deplasează la cel mai mare volum | |
| Temperatura | Crește | Absoarbe căldura și schimbă constanta de echilibru |
| Scădea | Eliberează căldură și schimbă constanta de echilibru | |
| Catalizator | Prezenţă | Reacția accelerează |
Acest principiu are o mare importanță pentru industria chimică, deoarece reacțiile pot fi manipulate și pot face procesele mai eficiente și mai economice.
Un exemplu în acest sens este procesul dezvoltat de Fritz Haber, care, folosind principiul lui Le Chatelier, a creat economic o cale pentru producerea de amoniac din azotul atmosferic.
Apoi, vom analiza echilibrul chimic conform legii lui Chatelier și modul în care perturbările îl pot modifica.
știu mai multe despre:
- Echilibrul chimic
- Echilibrul ionic
- Indicatori acid-bazici
Efect de concentrare
Atunci când există un echilibru chimic, sistemul este echilibrat.
Sistemul în echilibru poate suferi o perturbare atunci când:
- Creștem concentrația unui component al reacției.
- Reducem concentrația unui component al reacției.
Când adăugăm sau eliminăm o substanță din reacția chimică, sistemul se opune schimbării, consumând sau producând mai mult din acel compus, astfel încât echilibrul să fie restabilit.
Concentrațiile de reactanți și produse se modifică pentru a se adapta la un nou echilibru, dar constanta de echilibru rămâne aceeași.
Exemplu:
In balanta:
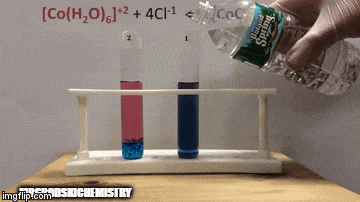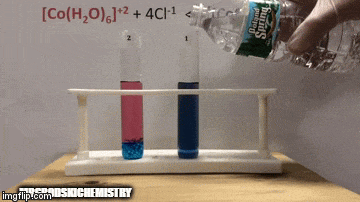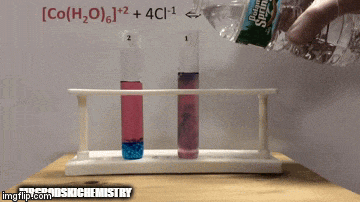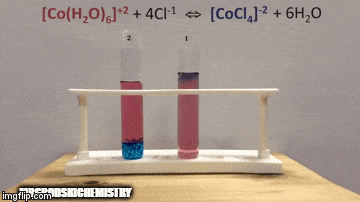
Reacția are o concentrație mai mare de produse, deoarece prin culoarea albastră a soluției vedem că complexul [CoCl4]-2 predomină.
Apa este, de asemenea, un produs al reacției directe și atunci când creștem concentrația sa în soluție, sistemul se opune schimbării, provocând reacția apei și a complexului.
Echilibrul este deplasat spre stânga, direcția inversă a reacției și determină creșterea concentrației reactanților, schimbând culoarea soluției.
Efectul temperaturii
Sistemul în echilibru poate suferi o perturbare atunci când:
- Există o creștere a temperaturii sistemului.
- Există o scădere a temperaturii sistemului.
Atunci când se adaugă sau se elimină energie dintr-un sistem chimic, sistemul se opune schimbării, absorbind sau eliberând energie, astfel încât echilibrul să fie restabilit.
Când sistemul variază temperatura, echilibrul chimic se modifică după cum urmează:
Prin creșterea temperaturii, reacția endotermică este favorizată și sistemul absoarbe căldura.
Pe de altă parte, când temperatura este redusă, reacția exotermă este favorizată și sistemul eliberează căldură.
Exemplu:
În echilibru chimic:
Când așezăm eprubeta care conține acest sistem într-un pahar cu apă fierbinte, temperatura sistemului crește și echilibrul se schimbă, formând mai multe produse.

Acest lucru se datorează faptului că reacția directă este endotermă și sistemul va fi restabilit prin absorbția căldurii.
În plus, variațiile de temperatură modifică și constantele de echilibru.
Efect de presiune
Sistemul în echilibru poate suferi o perturbare atunci când:
- Există o creștere a presiunii totale a sistemului.
- Există o scădere a presiunii totale a sistemului.
Când creștem sau micșorăm presiunea unui sistem chimic, sistemul se opune schimbării, deplasând echilibru în sensul unui volum mai mic sau respectiv mai mare, dar nu modifică constanta de echilibru.
Când sistemul variază volumul, acesta minimizează acțiunea presiunii aplicate, după cum urmează:
Cu cât este mai mare presiunea aplicată sistemului, va exista o contracție a volumului și echilibrul se deplasează către numărul mai mic de moli.
Cu toate acestea, dacă presiunea scade, sistemul se extinde, crescând volumul și direcția reacției este deplasată la cea cu cel mai mare număr de moli.
Exemplu:
Celulele corpului nostru primesc oxigen prin echilibrul chimic:
Acest sistem se stabilește atunci când oxigenul din aerul pe care îl respirăm intră în contact cu hemoglobina prezentă în sânge, dând naștere la oxi-hemoglobină, care transportă oxigenul.
Când o persoană urcă un munte, cu cât altitudinea este mai mare, cu atât este mai mică cantitatea și presiunea parțială a lui O2 sus în aer.
Echilibrul care transportă oxigenul în corp se deplasează spre stânga și reduce cantitatea de oxi-hemoglobină, compromitând cantitatea de oxigen primită de celule.
Rezultatul este apariția amețelilor și oboselii, care poate duce chiar la moarte.
Corpul încearcă să reacționeze producând mai multă hemoglobină. Cu toate acestea, acesta este un proces lent, care necesită setarea la altitudine.

Prin urmare, oamenii care pot urca pe Muntele Everest sunt cei care se potrivesc cel mai bine altitudinii extreme.
Catalizatori
Utilizarea unui catalizator interferează cu viteza de reacție, atât în reacția directă, cât și în cea inversă.
Pentru ca o reacție să apară, este necesar să se atingă o energie minimă pentru ca moleculele să se ciocnească și să reacționeze eficient.
Catalizatorul, atunci când este introdus în sistemul chimic, acționează prin scăderea acestei energii de activare formând un complex activat și creând o cale mai scurtă pentru a ajunge la echilibrul chimic.
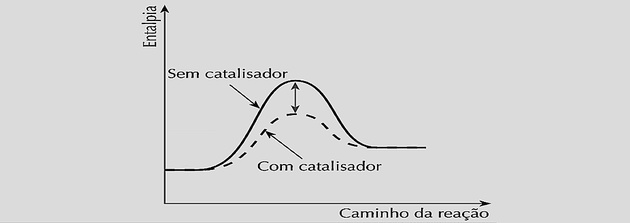
Prin creșterea vitezelor de reacție în mod egal, reduce timpul necesar pentru a ajunge la echilibru, așa cum se poate vedea în următoarele grafice:
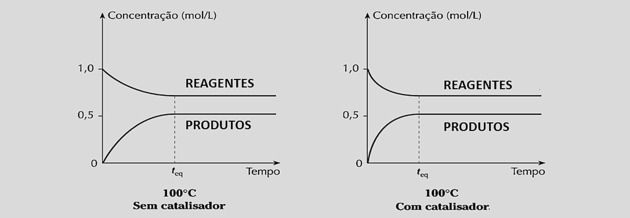
Cu toate acestea, utilizarea catalizatorilor nu modifică randamentul reacției sau constanta de echilibru, deoarece nu interferează cu compoziția amestecului.
sinteza amoniacului
Compușii pe bază de azot sunt folosiți pe scară largă în îngrășăminte agricole, explozivi, medicamente, printre altele. Datorită acestui fapt, se produc milioane de tone de compuși de azot, cum ar fi NH amoniac3, Azotat de amoniu NH4LA3 și uree H2NCONH2.
Datorită cererii mondiale de compuși de azot, în principal pentru activități agricole, salpetrul NaNO din Chile3, principala sursă de compuși azotați, a fost cea mai utilizată până la începutul secolului al XX-lea, dar săpătorul natural nu ar fi în măsură să satisfacă cererea actuală.
Este interesant de observat că aerul atmosferic este un amestec de gaze, compus din peste 70% azot N2. Cu toate acestea, datorită stabilității legăturii triple devine un proces foarte dificil de a rupe această legătură pentru a forma noi compuși.
Soluția acestei probleme a fost propusă de chimistul german Fritz Haber. Sinteza amoniacului propusă de Haber aduce următorul echilibru chimic:
Pentru a fi implementat industrial, acest proces a fost perfecționat de Carl Bosch și este cel mai folosit până în prezent pentru captarea azotului din aer, concentrându-se pe obținerea compușilor azotati.
Folosind principiul Le Chatelier, echilibrul chimic poate fi mărit atunci când:
Adăugați H2 și face ca sistemul să se opună schimbării și să reacționeze pentru a reduce concentrația acelui reactant.
Astfel, H2 si nu2 sunt consumate simultan pentru a produce mai mult produs și a crea o nouă stare de echilibru.
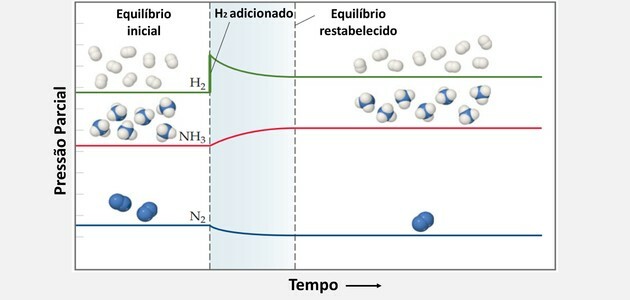
La fel, adăugând mai mult azot, echilibrul se deplasează spre dreapta.
Din punct de vedere industrial, echilibrul este mutat prin îndepărtarea continuă a NH3 a sistemului prin lichefierea selectivă, crescând randamentul reacției, deoarece echilibrul care urmează să fie restabilit tinde să formeze mai mult produs.
Sinteza Haber-Bosch este una dintre cele mai importante aplicații ale studiilor de echilibru chimic.
Datorită relevanței acestei sinteze, Haber a primit Premiul Nobel pentru chimie în 1918, iar Bosch a primit Premiul în 1931.
Exerciții de schimbare a echilibrului
Acum, că știi cum să interpretezi schimbările care pot apărea în echilibrul chimic, folosește aceste întrebări vestibulare pentru a-ți testa cunoștințele.
1. (UFPE) Cele mai potrivite antiacide ar trebui să fie cele care nu reduc prea mult aciditatea din stomac. Când reducerea acidității este prea mare, stomacul secretă excesul de acid. Acest efect este cunoscut sub numele de „revanșă acidă”. Care dintre elementele de mai jos ar putea fi asociat cu acest efect?
a) Legea conservării energiei.
b) Principiul excluderii Pauli.
c) Principiul Le Chatelier.
d) Primul principiu al termodinamicii.
e) Principiul incertitudinii lui Heisenberg.
Alternativă corectă: c) Principiul lui Le Chatelier.
Antiacidele sunt baze slabe care funcționează prin creșterea pH-ului stomacului și, în consecință, scăderea acidității.
Scăderea acidității are loc prin neutralizarea acidului clorhidric prezent în stomac. Cu toate acestea, prin reducerea acidității prea mult, poate crea un dezechilibru în organism, deoarece stomacul funcționează într-un mediu acid.
După cum se afirmă în principiul lui Le Chatelier, atunci când un sistem în echilibru este expus la o perturbare, va exista opoziție față de această schimbare, astfel încât echilibrul să fie restabilit.
În acest fel, organismul va produce mai mult acid clorhidric producând efectul de „revanșare a acidului”.
Celelalte principii prezentate în alternative se referă la:
a) Legea conservării energiei: într-o serie de transformări, energia totală a sistemului este conservată.
b) Principiul excluderii Pauli: într-un atom, doi electroni nu pot avea același set de numere cuantice.
d) Primul principiu al termodinamicii: variația energiei interne a sistemului este diferența dintre căldura schimbată și munca efectuată.
e) Principiul incertitudinii Heisenberg: nu este posibil să se determine viteza și poziția unui electron la un moment dat.
În ceea ce privește sistemul în echilibru, se poate afirma corect că:
a) prezența unui catalizator afectează compoziția amestecului.
b) prezența unui catalizator afectează constanta de echilibru.
c) creșterea presiunii scade cantitatea de CH4(g).
d) creșterea temperaturii afectează constanta de echilibru.
e) creșterea temperaturii scade cantitatea de CO(g) .
Alternativă corectă: d) creșterea temperaturii afectează constanta de echilibru.
Prin creșterea temperaturii, reacția directă, care este endotermă, va fi afectată, deoarece pentru a restabili echilibrul, sistemul va absorbi energia și va deplasa balanța spre dreapta.
Deplasarea balanței în direcția directă, crește cantitatea de produse formate.
Constanta de echilibru este direct proporțională cu concentrația produselor: cu cât este mai mare cantitatea de produse, cu atât este mai mare valoarea constantei.
Putem observa atunci că creșterea temperaturii crește cantitatea de CO și H2.
Creșterea presiunii mută echilibrul către reacția inversă, pe măsură ce echilibrul se deplasează către cel mai mic număr de moli. Cu aceasta, cantitatea de CH4 si H2Este mărită.
Utilizarea catalizatorului nu interferează cu constanta de echilibru și compoziția amestecului. Acesta va acționa doar prin realizarea echilibrului mai rapid.
3. (UFC) În studiul acțiunii gazelor otrăvitoare COCl2, folosit ca armă chimică, procesul de descompunere este observat în funcție de reacție:
Pornind de la o situație de echilibru, s-au adăugat 0,10 mol de CO și sistemul, după ceva timp, a ajuns la o nouă situație de echilibru. Alegeți opțiunea care indică modul în care noile concentrații de echilibru sunt legate de cele vechi.
| [COCI2] | [CO] | [Cl2] | |
| ) | nou> vechi | nou> vechi | nou |
| B) | nou> vechi | nou> vechi | nou> vechi |
| ç) | nou | nou> vechi | nou |
| d) | nou> vechi | nou | nou |
| și) | la fel | la fel | la fel |
Alternativă corectă:
| [COCI2] | [CO] | [Cl2] | |
| ) |
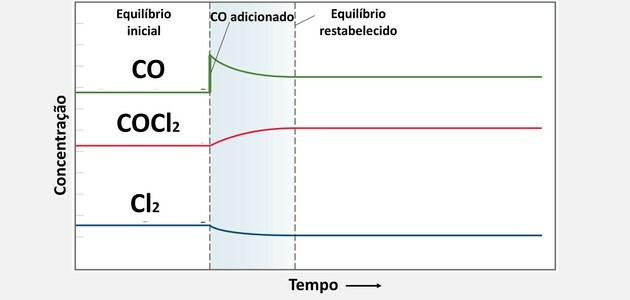
Când se adaugă o substanță nouă, sistemul consumă acea substanță pentru a restabili echilibrul, deoarece concentrația sa a crescut.
Acest consum are loc prin reacția substanței cu celălalt compus, creând astfel mai mult produs.
Prin urmare, atunci când creștem concentrația de CO, va exista consum, dar nu până la punctul de a deveni mai mică decât concentrația în starea inițială, deoarece consumul acesteia va avea loc împreună cu altul componentă.
Deja concentrația de Cl2 devine mai mic decât cel inițial, deoarece a trebuit să reacționeze cu cantitatea de CO adăugată.
De la joncțiunea celor două substanțe, concentrația de COCI a crescut2, deoarece este produsul format.
Aceste modificări ale echilibrului chimic pot fi văzute în următorul grafic:
4. (UFV) Studiul experimental al unei reacții chimice în echilibru a demonstrat că creșterea în temperatura a favorizat formarea produselor, în timp ce creșterea presiunii a favorizat formarea de reactivi. Pe baza acestor informații și știind că A, B, C și D sunt gaze, marcați alternativa care reprezintă ecuația studiată:
| ) | ||
| B) | ||
| ç) | ||
| d) | ||
| și) |
Alternativă corectă:
| ) |
Pe măsură ce temperatura crește, sistemul absoarbe căldura pentru a restabili echilibrul și, cu aceasta, favorizează reacția endotermică, a cărei ∆H este pozitivă.
Alternativele care corespund favorizării formării produselor prin creșterea temperaturii sunt: a, b și d.
Cu toate acestea, atunci când presiunea crește, echilibrul se deplasează spre cel mai mic volum, adică cel cu cel mai mic număr de moli.
Pentru ca reacția să fie deplasată spre reactanți, este necesar ca această direcție a reacției să aibă un număr mai mic de moli în raport cu produsele.
Acest lucru este observat numai în prima alternativă.
5. (UEMG) Următoarele ecuații reprezintă sisteme în echilibru. Care este singurul sistem care nu se schimbă prin schimbarea presiunii?
a) OS2 (g) + 1/2 O2 (g) ⇔ ASA3(g)
b) CO2 (g) + H2 (g) ⇔ CO(g) + H2O(g)
c) Nu2 (g) + 3 H2 (g) ⇔ 2 NH3(g)
d) 2 CO2 (g) ⇔ 2 CO(g) + O2 (g)
Alternativă corectă: b) CO2 (g) + H2 (g) ⇔ CO(g) + H2O(g)
Când un sistem modifică presiunea totală, echilibrul se restabilește odată cu modificarea volumului.
Dacă presiunea crește, volumul scade, deplasând echilibrul la cel mai mic număr de moli.
Pe de altă parte, când presiunea scade, volumul crește, deplasând balanța către un număr mai mare de moli.
Dar atunci când există același număr de moli de substanțe care reacționează și produse formate, nu există nicio modalitate de a schimba echilibrul, deoarece volumul nu se schimbă.
Știm numărul de aluniți după coeficienții stoichiometrici de lângă fiecare substanță.
Putem vedea acest lucru în ecuația alternativă
b) CO2 (g) + H2 (g) ⇔ CO(g) + H2O(g)
unde 1 mol de CO2 reacționează cu 1 mol de H2 pentru a forma 1 mol de CO și 1 mol de H2O.
În ambele direcții ale reacției există 2 moli, deci modificările presiunii nu ar schimba volumul.
Consultați mai multe întrebări despre deplasarea echilibrului chimic, cu rezoluție comentată, în această listă pe care am pregătit-o: exerciții de echilibru chimic.
Cine a fost Le Chatelier?