Se poate întâmpla să existe acizi din același element, iar acest element să aibă același număr de oxidare (NOX), dar diferența este în gradele de hidratare.
De exemplu, mai jos, avem trei acizi formați din elementul fosfor (P):
H3PRAF4 H4P2O7 HPO3
Rețineți că în toți cei trei acizi numărul de oxidare al fosforului este +5; diferența este în gradul de hidratare.
Pe baza acestora, acești acizi se diferențiază în nomenclatură prin prefixe orto, piro și meta.
Cel mai hidratat acid se numește orto. În exemplul dat, primul (H3PRAF4) se numește acid ortofosforic, deoarece este cel mai hidratat dintre cele trei. Prefixul orto este consumabil, deci de cele mai multe ori acest acid va fi numit doar acid fosforic.
Prefixele pyro și meta sunt utilizate cu orto acid ca punct de referință:
- Pyrus: 2 molecule de orto minus 1 moleculă de H2O
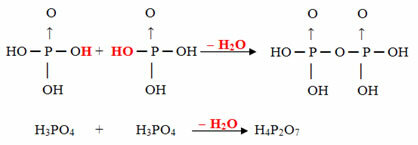
Exemplu: H4P2O7 se numește acid pirofosforic deoarece este egal cu două molecule de acid ortofosforic (H3PRAF4) minus o moleculă de apă.
2. H3PRAF4 = H6P2O8
H6P2O8 - H2O = H4P2O7
Acest proces este un deshidratare intermoleculară:
- Scop: 1 moleculă de orto minus 1 moleculă de H2O
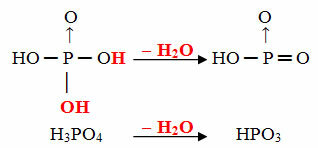
Exemplu: HPO3 se numește acid poartăfosforic deoarece este egal cu o moleculă de acid ortofosforic (H3PRAF4) minus o moleculă de apă.
H3PRAF4 - H2O = HPO3
Acest proces este un deshidratare intramoleculară:
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/grau-hidratacao-dos-acidos.htm


