Unul dintre modurile în care sunt organizate elementele chimice este prin familii, care corespund secvențelor verticale ale tabelului periodic.
La 18 coloane din tabel grupează elementele în funcție de asemănări în proprietățile chimice.
Organizarea elementelor chimice în familii a fost un mod practic de structurare a diverselor informații găsite și prezentarea lor într-un mod simplu.
Pentru a facilita localizarea unui element chimic, familiile au fost desemnate în număr de la 1 la 18 după cum urmează:
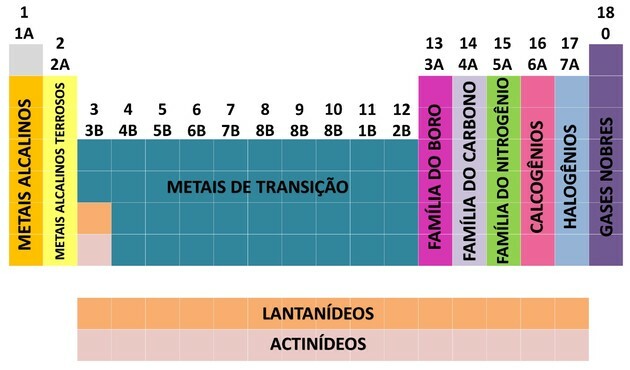
Prin contribuția multor oameni de știință și diferite încercări de aranjare a datelor, tabelul periodic a evoluat, stabilind o ordine de aranjare a elementelor.
Nomenclatorul familiilor
- Familiile din tabel au fost împărțite în A (reprezentativ) și B (tranziție), fiind identificate prin litere și cifre.
- Tu elemente reprezentative familiile 0, 1A, 2A, 3A, 4A, 5A, 6A și 7A corespund.
- Tu elemente de tranziție familiile 1B, 2B, 3B, 4B, 5B, 6B, 7B și 8B corespund.
- Prin determinarea Uniunii Internaționale de Chimie Pură și Aplicată (IUPAC), familiile au fost identificate în grupuri de la 1 la 18.
Tabel periodic și distribuție electronică
Asemănările dintre elementele aceleiași familii apar deoarece numărul de electroni de valență al atomului în starea de bază este același pentru membrii unui anumit grup.
De exemplu:
| Grupa 1 | Distribuție electronică |
|---|---|
| 3citit | 2-1 |
| 11La | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Pr | 2-8-18-32-18-8-1 |
Atomii grupului 1 au electronii distribuiți pe mai mult de un nivel de energie, dar toți au un electron de valență.
Cu aceasta, observăm că realizarea distribuție eletronică a atomului în starea fundamentală, găsim poziția acestuia pe tabelul periodic.
elemente reprezentative
Elementele reprezentative prezintă un comportament chimic relativ mai puțin complex decât elementele de tranziție și formează majoritatea substanțelor din jurul nostru.
Unele familii de elemente reprezentative primesc nume speciale, după cum se arată mai jos:
grup |
Familie | nume specific | Denumirea originii | Elemente | configurație electronică |
|---|---|---|---|---|---|
| 1 | 1A | Metale alcaline | din latină alcalin, care înseamnă „gri de plante”. | Li, Na, K, Rb, Cs și Fr | ne1 |
| 2 | 2A | metale alcalino-pământoase | Termenul „pământean” se referă la „existent pe pământ”. | Fii, Mg, Ca, Sr, Ba și Ra | ne2 |
| 13 | 3A | familia borului | Numele primului element al familiei. | B, Al, Ga, In, Tl și Nh. | ne2np1 |
| 14 | 4A | familia carbonului | Numele primului element al familiei. | C, Si, Ge, Sn, Pb și Fl. | ne2np2 |
| 15 | 5A | Familia azotului | Numele primului element al familiei. | N, P, As, Sb, Bi și Mc. | ne2np3 |
| 16 | 6A | Chalcogeni | din greacă khalks, deoarece sunt elemente găsite în minereurile de cupru. | O, S, Se, Te, Po și Lv. | ne2np4 |
| 17 | 7A | Halogeni | Expresie greacă care înseamnă formatori de sare. | F, Cl, Br, I, At și Ts. | ne2np5 |
| 18 | 0 | Gaze nobile | S-a considerat că nu reacționează cu alte substanțe. | El, Ne, Ar, Kr, Xe, Re și Og. | 1s2 (El) sau noi2np6 |
Prin tabel, putem vedea că:
- Elementele prezentate mai sus sunt clasificate ca reprezentative deoarece au cel mai energic electron într-un subnivel s sau p.
- Electronii sunt distribuiți pe niveluri de energie și n reprezintă nivelul cel mai exterior al atomului în starea fundamentală.
- Elementele reprezentative, conform recomandării IUPAC, aparțin grupurilor sau familiilor 1,2,13,14,15,16,17 și 18.
O hidrogen este clasificat în afară de celelalte elemente. Chiar și cu configurația electronică 1s1, el nu face parte din grupul 1 pentru că prezintă un comportament singular.
elemente de tranziție
Elementele de tranziție corespund grupelor 3-12. Ei primesc acest nume deoarece au caracteristici intermediare între grupurile 1 și 2 și elementele reprezentative nemetalice.
Tu metale de tranziție sunt definite de IUPAC ca:
Un element de tranziție are un subnivel d incomplet sau poate forma cationi cu un subnivel d incomplet.
Când cel mai energic electron al atomului în starea fundamentală se află într-un subnivel incomplet, este caracterizat ca o tranziție externă.
Lantanidele și actinidele sunt elemente de tranziție interne deoarece au cel puțin un subnivel incomplet.
Atunci când elementele au electroni care umple orbitalii d sau f, acestea prezintă proprietăți similare și pot fi clasificate în elemente de tranziția exterioară sau interioară.
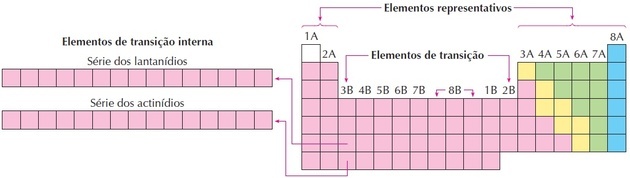
După cum putem vedea în imagine, familia 8B corespunde a 3 coloane, acestea sunt grupurile 8, 9 și 10, care au fost grupate astfel, deoarece au caracteristici similare.
Principalele caracteristici ale familiilor
Tabelul de mai jos prezintă principalele proprietăți ale grupurilor din tabelul periodic:
| grup | Caracteristici | substanțe compuse mai frecvente |
apariții |
|---|---|---|---|
| 1 | Solid și strălucitor în condiții ambientale. Conductori de energie electrică foarte reactivi, moi și buni. | Săruri, hidroxizi și oxizi |
Reacționează cu halogeni și formează săruri. |
| 2 | Mai puțin reactiv și mai greu decât grupul 1. Solid argintiu cu o conductivitate bună. | Săruri, hidroxizi și oxizi |
Formând săruri și oxizi. |
| 3-12 | Ele formează complexe. Sunt solide metalice, dure și fragile, cu excepția mercurului, care este un lichid. | Săruri, oxizi și complexe. Ex: AgNO3, TiO și [Cr (OH)3(H2O)3] |
În minerale sub formă de oxizi. |
| 13 | Solid în condiții ambientale, argintiu, cu excepția borului. | Oxizi Ex: B2O3 |
În minerale sub formă de oxizi. |
| 14 | Solid în condiții ambientale. | Atomii de C și Si se pot aranja în lanțuri și pot produce o mare varietate de substanțe. | În organismele vii și sub formă de silicați sau oxizi. |
| 15 | Solidele, cu excepția azotului, care este gazos în condiții ambientale. | Oxizi și acizi Ex: NU2 si H3PRAF4 |
Atmosferă, organisme vii și minerale. |
| 16 | Solidele, cu excepția oxigenului, care este gazos în condiții ambientale. | Sulfuri și oxizi Ex: ZnS și SiO2 |
Atmosferă, organisme vii și minerale. |
| 17 | Acestea formează molecule diatomice și sunt foarte reactive. Sunt conductori răi ai electricității și căldurii. Sunt agresivi pentru ființele vii și pentru mediu. | Acizi și săruri. Ex: HCl și KBr |
Sunt prezente în substanțe organice și minerale. |
| 18 | Sunt foarte stabile și se găsesc sub formă de gaze. | Cu greu formează substanțe compuse. | Gazele din atmosferă. |
Proprietățile chimice și fizice disting o familie de alta. După cum am văzut, proprietățile chimice sunt legate de electroni de valență, și prin intermediul acestora, un atom interacționează cu altul, fiind responsabil pentru comportamentul chimic și legături chimice format.
Proprietățile fizice ale elementelor din același grup pot varia în funcție de numărul atomic și de masă.
Exerciții
Acum, că știți puțin mai multe despre familiile Tabelului periodic, testați-vă cunoștințele și vedeți ce ați învățat.
1) Luați în considerare următorul extract din Tabelul periodic.
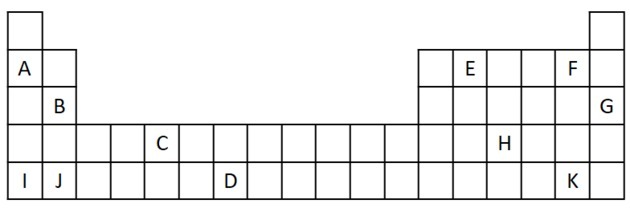
a) Numiți două elemente care au doi electroni de valență.
b) Indicați un element care reacționează violent cu apa, producând un hidroxid metalic.
c) Indicați un element non-reactiv.
d) Indicați două elemente care se combină cu metale alcaline pentru a forma săruri.
Răspuns:
a) B și J
Doi electroni de valență corespund grupei 2, care are o configurație ns electronică2 și sunt reprezentate în exercițiu de B și J.
b) A, B, I sau J.
A și I reprezintă elemente ale familiei 1; B și J provin din familia 2. După cum am văzut în tabelul cu proprietăți, elementele grupului 1 și 2 sunt foarte reactive și pot forma hidroxizi, ca în exemplele date: KOH și Mg (OH)2.
c) G
Gazele nobile sunt foarte stabile și, prin urmare, nu sunt foarte reactive. Litera G este inserată în tabel ca element al acestei familii.
d) F și K
Halogenii reacționează cu metalele alcaline pentru a forma săruri. Cel mai frecvent exemplu în acest sens este sarea de masă, NaCI.
2) Figura următoare prezintă trei elemente chimice, de la stânga la dreapta, litiu, sodiu și potasiu.

Selectați opțiunea care completează corect fiecare dintre următoarele afirmații.
1.1) „Putem spune că litiu, sodiu și potasiu ...
(A)... aparțin aceleiași perioade. ”
(B)... are același număr atomic. ”
(C)... aparțin aceluiași grup. ”
(D)... are același număr de masă. ”
1.2) „Elementele litiu, sodiu și potasiu ...
(A)... are proprietăți chimice foarte similare. ”
(B)... are proprietăți chimice foarte diferite. ”
(C)... sunt nemetale. ”
(D)… reacționează cu apa pentru a forma soluții acide. ”
Răspunsuri:
1.1) (C) aparțin aceluiași grup.
1.2) (A) are proprietăți chimice foarte similare.
Putem obține aceste informații consultând tabelul periodic sau realizând distribuția electronică a elementelor litiu, sodiu și potasiu. Vom vedea că cei trei au un electron în învelișul de valență și, deoarece fac parte din același grup, proprietățile chimice sunt foarte similare.
3) Luați în considerare următorul tabel, unde sunt reprezentate numerele atomice și distribuțiile electronice ale unor elemente chimice.
| Element | simbol chimic | numar atomic | Distribuție electronică |
|---|---|---|---|
| Litiu | citit | 3 | 2,1 |
| Beriliu | fi | 4 | 2,2 |
| Fluor | F | 9 | 2,7 |
| neon | Huh | 10 | 2,8 |
| clor | Cl | 17 | 2,8,7 |
| argon | Aer | 18 | 2,8,8 |
| Potasiu | K | 19 | 2,8,8,1 |
| Calciu | Aici | 20 | 2,8,8,2 |
Indicați grupul fiecărui element.
Răspuns:
Litiu și potasiu: grupa 1. (Au un electron în învelișul de valență).
Beriliu și calciu: grupa 2. (Au doi electroni în învelișul de valență).
Fluor și clor: grupa 17. (Au șapte electroni în cochilia de valență).
Neon și argon: grupa 18. (Au opt electroni în carcasa de valență).
Verificați întrebările la examenul de admitere cu o rezoluție comentată în Exerciții pe tabelul periodic și întrebări nepublicate pe această temă în Exerciții de organizare a tabelului periodic.


