THE distilare, în general, este una dintre cele mai utilizate metode pentru despărțire componentele amestecurilor omogene care prezintă lichid cu solid sau numai lichide în compoziția lor.
Apelul distilație fracțională este utilizat exclusiv pentru a separa componentele unui amestec care are două sau mai multe lichide în constituția sa, cum ar fi un amestec de apă și acetonă. Este important ca lichidele care alcătuiesc amestecul să nu aibă puncte de fierbere prea apropiate sau să amestecul nu este azeotrop (amestec omogen format numai din lichide care are punctul de fierbere constant). În aceste două cazuri, sunt necesare metode chimice pentru separare.
Echipament utilizat într-o distilare fracționată acestea sunt practic aceleași ca și pentru o distilare simplă, cu adăugarea unui echipament numit coloană de fracționare. Vedeți-le pe toate mai jos:
Trepied de fier: susține ecranul de azbest și balonul de sticlă;
Arzător Bunsen: echipamente care efectuează încălzirea amestecului;
-
Ecran de azbest:
echipament care este poziționat pe trepied astfel încât să absoarbă o parte din căldura provenită de la arzătorul bunsen, împiedicând explozia balonului de distilare;
Observare: setul de ecran de azbest, trepiedul de fier și arzătorul cu bunsen pot fi înlocuite cu o placă electrică de încălzire.
Balon de sticlă:echipament de sticlă care primește amestecul omogen compus din lichide;

Coloana de fracționare:tub de sticlă umplut cu marmură de sticlă sau porțelan.

Condensator: echipament în care vaporii sunt transformați în lichid.

Erlenmeyer sau orice alt tub de colectare: echipament de sticlă care primește lichidul care a fost condensat în condensator.

Termometru:echipament care permite monitorizarea temperaturii în timpul procesului de distilare.

Cum funcționează o distilare fracționată se bazează pe diferența de Punct de fierbere între lichidele care alcătuiesc amestecul. Să folosim exemplul de apă (punctul de fierbere egal cu 100 OC) și acetonă (punctul de fierbere egal cu 58 OC) să înțeleagă cum funcționează acest proces.
Inițial adăugăm amestecul în balonul de sticlă. Apoi aprindem arzătorul bunsen sau placa de încălzire pentru a încălzi amestecul. De acolo, cele două lichide încep să se transforme în vapori și se îndreaptă spre coloana de fracționare, unde concurează pentru același spațiu. Deoarece coloana de fracționare este un obstacol, deoarece conține mai multe bile și puțin spațiu liber, doar unul dintre vapori este capabil să o traverseze. Doar vaporii lichizi care au cel mai scăzut punct de fierbere trec prin coloana de fracționare, deoarece cu cât este mai scăzut punctul de fierbere, cu atât este mai mică densitatea vaporilor. După trecerea prin coloana de fracționare, vaporii lichizi cu un punct de fierbere mai mic pătrund în condensator și suferă fenomenul de condensare, revenind la starea lichidă. În cele din urmă, lichidul condensat este colectat în balonul de colectare. Următoarea imagine prezintă o schemă de distilare fracționată:
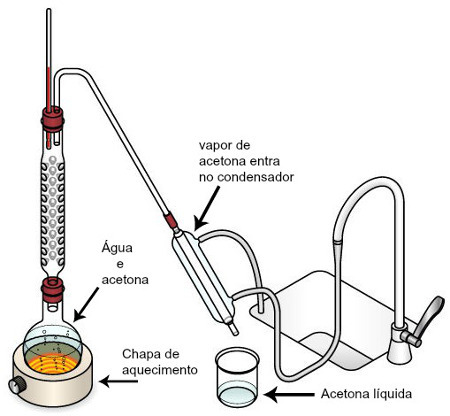
Ilustrație de distilare fracționată
Ca și în exemplul utilizat, acetona are cel mai scăzut punct de fierbere, este cea care reușește să traverseze coloana de fracționare, fiind condensată și colectată în balonul colector.
Observare: Pentru a preveni trecerea vaporilor de apă și prin coloana de fracționare, este important să rămâneți întotdeauna aprins priviți termometrul și nu permiteți ca temperatura de încălzire să depășească valoarea celui mai scăzut punct de fierbere.
De mine. Diogo Lopes Dias
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/destilacao-fracionada.htm



