Unii compuși au în structura lor legături duble alternând cu legături simple. Cel mai faimos dintre toate este benzenul, a cărui structură a fost propusă în 1865 de chimistul german Friedrich August Kekulé (1829-1896). Structura sa ar fi ciclică și formată din trei legături duble intercalate cu trei legături simple, așa cum se arată în figurile de mai jos:
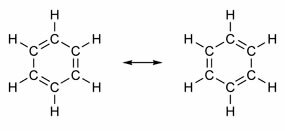
Ambele moduri de reprezentare a benzenului sunt acceptabile, deoarece este posibil să se schimbe electronii din legăturile π fără a schimba poziția atomilor. Cu toate acestea, nici unul nu reprezintă exact ceea ce este și nici nu își explică comportamentul. Ar trebui să se comporte ca o alchenă și să provoace reacții de adăugare, dar în practică acest lucru nu se întâmplă. Benzenul este destul de stabil și acționează ca și cum nu ar avea legături duble; dă reacții de substituție ca în alcani.
În 1930, omul de știință american Linus Pauling a propus teoria rezonanței care explica această aparentă contradicție. Această teorie spunea:
„Ori de câte ori, într-o formulă structurală, putem schimba poziția electronilor fără a schimba poziția atomilor, structura reală Nu nu va fi niciuna dintre structurile obținute, ci mai degrabă a hibrid de rezonanță a acestor structuri. ”
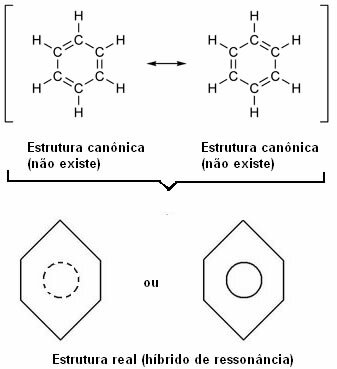
Acest efect este evidențiat de dimensiunea legăturilor de carbon și de distanța dintre ele. Această distanță este intermediară față de cea a legăturii simple (1,54 Å) și a legăturii duble (1,34 Å); fiind, deci, 1,39 Å, datorită efectului de rezonanță.
Acest efect poate fi observat și în structura moleculei de ozon (O3), așa cum se arată mai jos:
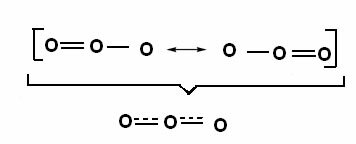
Structuri canonice și hibrizi de rezonanță a ozonului.
De Jennifer Fogaça
Absolvent în chimie
Echipa școlii din Brazilia.
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/ressonancia-compostosquimicos.htm

