Antoine Laurent din Lavoisier s-a născut la 26 august 1743, la Paris.Tatăl său era un avocat bogat, iar mama lui a murit la începutul vieții sale. Tatăl și mătușa l-au trimis la Colégio Mazzarino pentru a studia dreptul.Cu toate acestea, el a avut un interes mai mare în domeniul științei.
La 22 de ani și-a arătat deja marea ingeniozitate proiectând un proiect de iluminat pentru străzile din Paris, pentru care a câștigat o medalie de aur de la Academia de Științe.La vârsta de 25 de ani, a fost ales membru al prestigioasei Academii Regale de Științe din Franța.
La aceeași vârstă, a cumpărat acțiuni la Ferme Générale, asociindu-se cu acea instituție privată care colecta impozite de la oameni în numele coroanei franceze. Scopul său a fost de a acoperi costurile experimentelor și cercetărilor sale.
La vârsta de 26 de ani, a cunoscut-o pe Marie Anne Pierrette Paulze (1758-1836), care era fiica unuia dintre partenerii majori ai Ferme Générale. Lavoisier și Marie Anne s-au căsătorit când ea avea doar 13 ani, iar el avea 29 de ani. Dar această căsătorie s-a transformat într-o mare uniune între ei, deoarece Marie Anne l-a ajutat pe Lavoisier în cercetările sale, fiind partenerul și asistentul său.
Ea l-a ajutat prin asamblarea aparatului pentru experimentele sale, precum și prin traducerea lucrărilor științifice și filosofice.

Lavoisier și soția și asistenta sa, Marie Anne
Lavoisier a fost unul dintre marii oameni de știință din istorie, fiind considerat de mulți ca fiind tată al chimiei moderne. El a făcut observații detaliate și, spre deosebire de majoritatea, și-a planificat cu atenție experimentele, măsurând masa materialelor înainte și după transformări chimice.

Ilustrație a laboratorului lui Lavoisier unde experimenta cu ajutorul soției sale (care este așezată în dreapta, luând notițe)
Printre principalele sale descoperiri, putem evidenția:
* Descoperirea oxigenului și relația dintre respirație și reacția de ardere:În 1774 Priestley descoperise un gaz nou, cu care Lavoisier a început să studieze și să experimenteze. Cu datele obținute, el a demonstrat că gazul nou era necesar pentru ca arderea să aibă loc, adică fără prezența sa, nu a existat nici o ardere.
Lavoisier a numit acest gaz oxigen, cuvânt din greacă oxi, care înseamnă „acid” și gen, „Generator sau producător”. El l-a numit pentru că experimentele sale l-au determinat să concluzioneze că acest gaz nou era prezent în toți acizii, care ulterior s-au dovedit a fi o concluzie greșită, dar totuși numele a ramas.
Pentru a vedea cât de adevărată este această descoperire de Lavoisier, aprindeți o lumânare și apoi acoperiți-o cu un flacon de sticlă. În timp, veți vedea că lumânarea se va stinge, deoarece tot oxigenul din sticlă va fi consumat la arderea lumânării și se va epuiza.
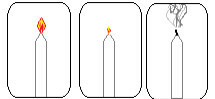
Experiment cu lumânări pentru a confirma descoperirea lui Lavoisier
* Compoziția aer: Lavoisier a arătat că același gaz (oxigen) făcea parte din aerul atmosferic și era gazul pe care îl respirăm. El a mai arătat că aerul atmosferic era un amestec de oxigen cu un alt gaz care nu participa la reacția de ardere. Astăzi știm că celălalt gaz este azot.
Aceste descoperiri ale lui Lavoisier au reprezentat o revoluție pentru ideile vremii despre transformările chimice și au debutat teoria lui flogiston, care era o teorie conform căreia fiecare substanță inflamabilă (arzătoare) conținea flogistonul - un misterios fluid pierdut în acest moment. de ardere.
* Legea conservării în masă sau legea lui Lavoisier: Lavoisier a arătat că, în reacțiile de ardere, masele tuturor substanțelor implicate au rămas neschimbate, adică masa că a cântărit la început, înainte de reacție, a fost la fel ca la sfârșitul reacției, atâta timp cât reacția a fost făcută într-un recipient închis. Cu asta, a ajuns la faimosul Legea conservării masei, care spune că, într-o reacție chimică, masa reactanților este egală cu masa produselor.
Astăzi această lege este cunoscută mai ales prin următoarea afirmație:
„În natură nu se creează nimic, nu se pierde nimic, totul se transformă”.
* Compoziția apei: Lavoisier a arătat, în 1783, că apa a fost rezultatul combinației a două părți de hidrogen și una de oxigen (H2O);
* Metabolizarea animalelor: Antoine Lavoisier a arătat că metabolismul animalelor a fost o combustie internă, în care carbonul iar hidrogenul care a fost obținut din alimente a reacționat cu oxigenul și a produs dioxid de carbon și Apă.
* Nomenclatura modernă pentru elemente: În 1789, Lavoisier a lansat lucrarea intitulată Tratatul de chimie elementară, în care a furnizat o nomenclatură modernă pentru 33 de elemente, care, conform conceptului corect de astăzi, sunt de fapt substanțe. Acest lucru era important, deoarece alchimia folosea un limbaj obscur pentru a se referi la elemente.
Din păcate, Lavoisier a ajuns la un sfârșit tragic. În același an din 1789 a avut loc Revoluția franceză, care a răsturnat ordinea politică existentă. Oamenii s-au răzvrătit împotriva exceselor coroanei, iar membrii Fermei Generale erau considerați dușmani, printre care și Lavoisier.
A fost arestat în noiembrie 1793 și, la 8 mai 1794, a fost ghilotinat în mijlocul Place de la Révolution din Paris, acum Place de la Concorde.

Obelisc egiptean la situl revoluționar de ghilotină din centrul Place de la Concorde pe 9 iunie 2014 la Paris, Franța *
* Imagine cu credit editorial: Veniamin Kraskov / Shutterstock.com
De Jennifer Fogaça
Absolvent în chimie



