La legaturi covalente, numit si legături moleculare sau homopolare, sunt cele care apar între atomii de elemente electronegative, adică cu tendința de a primi electroni, stabilind o legătură de împărțind electroni din cochiliile lor de valență.
Legătura covalentă poate avea loc între următoarele elemente: hidrogen, nemetale și semimetale. Metalele nu participă niciodată la acest tip de legătură.
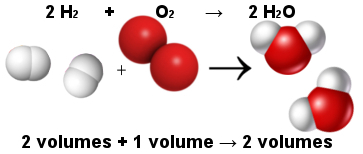
Să luăm în considerare un exemplu simplu de legătură covalentă: legătura formatoare de hidrogen gazos (H2):
H + H → H2
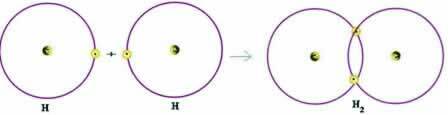
Rețineți că ambii atomi aveau nevoie pentru a primi un electron pentru a-și finaliza învelișul de valență - conform Regulii Octet - și, în acest fel, pentru a rămâne stabili. Prin urmare, și-au împărțit electronii și, în acest fel, amândoi aveau doi electroni, aveau carcasa lor completă K și obțineau configurația gazului nobil heliu.
Această împărțire a electronilor este ceea ce diferențiază acest tip de legătură de legătura ionică, în care are loc transferul de electroni.
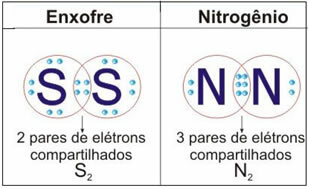
Vedeți figura de mai jos pentru alte două exemple ale acestui caz:
Nu te opri acum... Există mai multe după publicitate;)
În acest tip de legătură există formarea de molecule, care pot fi reprezentate de respectivele lor formule moleculare, adică cea mai simplă reprezentare care indică câți atomi din fiecare element sunt în moleculă. Câteva exemple de formule moleculare sunt: H2, S2, O2, Nu2, H2O, CO2, etc.
Legătura covalentă poate fi reprezentată de alte două formule:
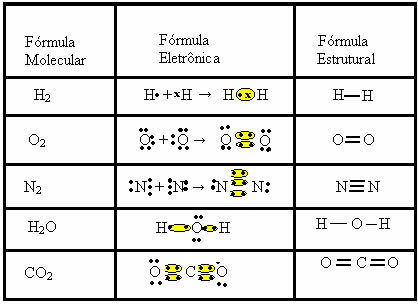
- Formula electronică sau Formula Lewis: în această formulă apar și electronii învelișului de valență al fiecărui atom și formarea perechilor electronice. Acești electroni sunt simbolizați prin semne . sau x;
- Formula structurală plană sau Formula structurală Couper: arată legăturile elementelor, fiecare pereche partajată corespunzând unei liniuțe. Dacă este doar o liniuță, îl numim un singur link; dacă există două, dublă legătură; iar dacă există trei liniuțe, triplă legătură.
Observați alte exemple de legături covalente reprezentate de aceste trei formule chimice:
De Jennifer Fogaça
Absolvent în chimie
Doriți să faceți referire la acest text într-o școală sau într-o lucrare academică? Uite:
FOGAÇA, Jennifer Rocha Vargas. "Legaturi covalente"; Școala din Brazilia. Disponibil in: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. Accesat la 27 iunie 2021.