Denumirea chimică a Vitamina C é Acid L-ascorbic, sau pur și simplu Acid ascorbic. Acest nume transmite rolurile chimice și biologice ale acestui compus. Aspectul chimic este că este acid, deoarece conține în structura sa o grupare fenolico-hidroxi. Grupul fenolic atașat celui de-al treilea carbon din lanț suferă ionizare în soluție apoasă, așa cum se arată mai jos, eliberând ionul hidroxon (H3O+), care este caracteristic comportamentului acid:
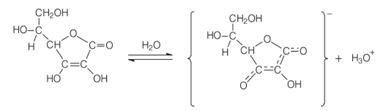
Cuvântul „ascorbic” provine din proprietatea sa biologică de a combate boala numită scorbut. Iar „L” provine din faptul că acidul ascorbic are un centru asimetric la carbonul 5, având activitate optică. Cu toate acestea, activitatea sa anti-scorbut derivă aproape în totalitate din izomerul L (levogir), care are o rotație specifică în apă de 24 °.
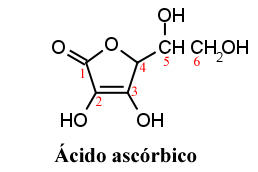
Acidul ascorbic a fost izolat pentru prima dată de cercetătorul maghiar Szent-Györgi în 1922 sub formă de pulbere cristalină albă.
Oamenii și alte animale, cum ar fi maimuțele, unele păsări și unii pești nu pot sintetiza vitamina C. Deficiența acestei vitamine în organism duce la sinteza defectuoasă a țesutului colagen și a bolii menționate mai sus
scorbut.Între principalele surse de vitamina C, avem fructe proaspete, precum cireșe, caju, guava, coacăze negre, mango, portocale, acerola, roșii, printre altele. Cartofii sunt, de asemenea, o sursă excelentă de vitamina C, la fel ca ardeii și legumele cu frunze (bertalha, broccoli, kale, napi, frunze de manioc și igname).

Spunem „fructe proaspăt”Deoarece vitamina C poate fi parțial sau complet distrusă în perioade lungi de depozitare. De exemplu, în fiecare lună stocată, cartoful pierde 15% din vitamina C. În plus, căldura îl poate distruge. Alimentele gătite lung și alimentele care au suferit prelucrări industriale conțin puțină vitamină C. În cazul cartofilor, dacă este gătit fără piele, va pierde imediat 30% până la 50% din proprietatea sa.
Una dintre principalele proprietăți ale acidului ascorbic este capacitatea sa de a acționa ca agent reducător. Deoarece are o ușurință excepțională de a fi oxidat într-o soluție apoasă, este un agent puternic antioxidant, deoarece se poate oxida în locul altor compuși.
De exemplu, în viața de zi cu zi, când tăiem anumite fructe, cum ar fi perele, bananele și merele, acestea se întunecă în timp. Acest lucru se datorează faptului că aceste fructe conțin enzima polifenol oxidază, care determină oxidarea enzimatică a compușilor fenolici naturali în prezența oxigenului molecular, formând chinone. Acestea polimerizează și generează melanine, care sunt exact pigmenții întunecați, insolubili pe care îi vedem că se formează în aceste fructe.
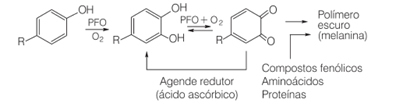
Una dintre modalitățile de inhibare a acțiunii enzimei polifenol oxidazei este adăugarea acidului ascorbic. Acest lucru se face, de exemplu, atunci când adăugăm suc de portocale în salata de fructe.
În prezența oxigenului și a unui catalizator, acidul ascorbic se oxidează, devenind acid dehidroascorbic. Acest acid are un pH sub 4, iar o scădere a pH-ului țesutului fructului face ca reacția de rumenire să încetinească. La pH sub 3, nu există activitate enzimatică.
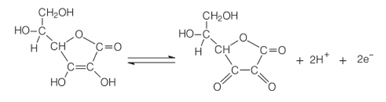
Această proprietate a vitaminei C este utilizată pe scară largă în industria alimentară pentru a preveni apariția gustului neplăcut, a toxicității și din motive economice, deoarece estimează că aproximativ 50% din pierderile de fructe tropicale din lume se datorează enzimei polifenol oxidaza.
Datorită rolului său antioxidant, vitamina C este, de asemenea, utilizată în produse cosmetice. Aplicarea sa actuală prin intermediul acestor produse cosmetice îi permite să atingă niveluri care nu sunt posibile doar cu aportul oral de vitamina C. Protejează pielea împotriva razelor UV și a radicalilor liberi care duc la îmbătrânirea prematură.

De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/composicao-aplicacoes-vitamina-c.htm

