În 1874, chimistul olandez Jacobus Henrique van’t Hoff (1852-1911) și chimistul francez Joseph Achille le Bel (1847-1930), prin teorii matematice, a sugerat independent existența carbonilor asimetric.
La acea vreme, ei au fost puternic criticați, mai ales van’t Hoff, de celebrul chimist german Adolph Wilhelm Kolbe (1818-1884). Cu toate acestea, Kolbe s-a înșelat, astăzi știm că există un carbon asimetric, atât de mult încât, în 1901, van’t Hoff a fost primul chimist care a primit Premiul Nobel.
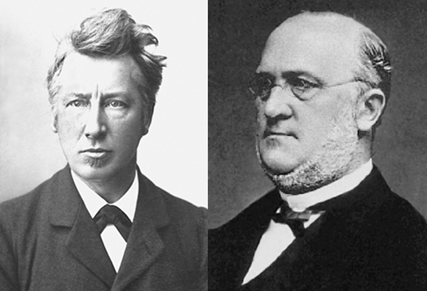
van’t Hoff (stânga) și Kolbe (dreapta)
Una dintre condițiile necesare pentru ca molecula să aibă activitate optică este ca aceasta să fie asimetrică. De asemenea, o modalitate de a verifica dacă este asimetrică este de a studia în detaliu structura sa pentru a vedea dacă are cel puțin un carbon asimetric.
Ce este o moleculă asimetrică și un carbon asimetric?
Ceva simetric este ceva care are cel puțin un plan de simetrie. De exemplu, dacă tăiem o rachetă de tenis în jumătate, cele două părți rezultate vor fi exact aceleași. Mai mult, dacă le așezăm în fața unei oglinzi plate, ele vor produce o imagine identică.
Se numesc structuri care nu suportă un plan de simetrie asimetric. Un exemplu este mâna noastră, deoarece dacă o așezăm în fața unei oglinzi, aceasta va produce o imagine diferită despre ea însăși. Dacă punem mâna dreaptă, imaginea va fi mâna stângă și invers. Un alt punct important este că nu se suprapun.
Nu te opri acum... Există mai multe după publicitate;)
De aceea se mai numește carbon asimetric carbon chiral, de unde provine acest cuvânt khéir care în greacă înseamnă mână.
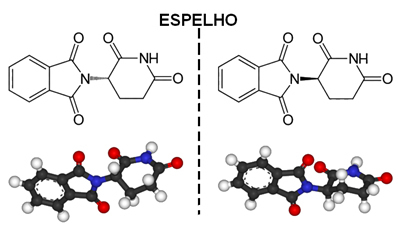
Un exemplu de moleculă asimetrică este talidomida, a cărei structură este prezentată mai jos:

Punctul situat cu un asterisc (*) corespunde unui carbon asimetric, ca și el are patru legături covalente care sunt realizate cu atomi sau grupuri de atomi diferiți.
Mai jos este un carbon cu patru liganzi diferiți în fața unei oglinzi. Rețineți că imaginea nu poate fi suprapusă peste structura originală:

Cele două molecule obținute mai sus sunt izomeri optici sau enantiomeri.
Revenind la cazul talidomidei, datorită faptului că are carbon asimetric, rezultatul este că molecula începe să aibă o imagine care nu se suprapune, care corespunde unei alte substanțe. Deci avem doi izomeri ai talidomidei cu proprietăți extrem de diferite.
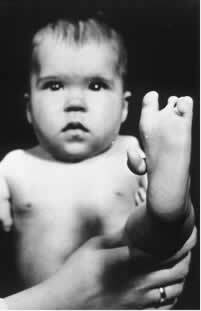
Unul dintre acești izomeri (R) are proprietăți sedative. Prin urmare, la sfârșitul anilor 1950, a început să fie folosit ca tranchilizant și ajutor de somn pentru femeile însărcinate. Acest lucru a declanșat o tragedie, deoarece enantiomerii săi (S) au fost, de asemenea, amestecați cu medicamentul. Acest izomer, la rândul său, este teratogen și a determinat multe femei însărcinate să își aibă bebelușii cu mâinile, picioarele, brațele și picioarele atrofiate.
De Jennifer Fogaça
Absolvent în chimie
Doriți să faceți referire la acest text într-o școală sau într-o lucrare academică? Uite:
FOGAÇA, Jennifer Rocha Vargas. „Carbon asimetric sau chiral”; Școala din Brazilia. Disponibil in: https://brasilescola.uol.com.br/quimica/carbono-assimetrico-ou-quiral.htm. Accesat la 27 iunie 2021.