Carbonații sunt compuși anorganici formați prin legarea ionică a unui metal sau semimetal cu anionul carbonat, CO32-.
Carbonul este tetravalent, adică are patru electroni în învelișul de valență și poate face patru legături covalente pentru a fi stabile, în timp ce oxigenul este bivalent, având șase electroni în coaja de valență și fiind capabil să facă două legături pentru a fi stabil, cu opt electroni. Astfel, există o puternică tendință ca un carbon să se lege de doi atomi de oxigen, care sunt stabili (O ═ C ═ O → CO2).
Dar alt oxigen se poate combina cu carbonul, deoarece raportul razelor ionice duce la un număr de coordonare egal cu 3, formând o structură triunghiular în care carbonul este în centru, formând o legătură dublă cu unul dintre atomii de oxigen și două legături simple cu ceilalți doi oxigenii. Rezultatul este doi electroni în exces, deoarece acești doi oxigeni nu sunt stabili, având nevoie să primească câte un electron:
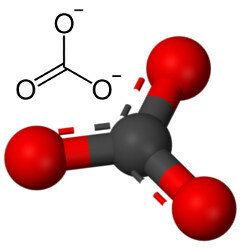
Anionul carbonat este format din legături covalente, dar compușii săi, care sunt săruri anorganice și minerale cunoscute sub numele de carbonați, sunt ionice, deoarece acest radical primește doi electroni de la un metal sau semimetal, formând un legătură ionică.
Acești compuși sunt insolubili în apă, cu excepția carbonatului de amoniu ((NH4)2CO3) și carbonați formați cu metale alcaline (elemente din familia 1: Li, Na, K, Rb, Cs și Fr). Aproape toate sunt solide albe, așa cum se arată în imaginea de mai jos:

Cele mai frecvente și mai importante exemple de zi cu zi de carbonați sunt carbonatul de sodiu (Na2CO3) și carbonat de calciu (CaCO3). În primul caz, sodiul aparține familiei 1, având un electron în învelișul de valență și tinde să piardă acest electron pentru a deveni stabil. Deoarece anionul carbonat trebuie să primească doi electroni, se leagă de doi atomi de sodiu:
Nu te opri acum... Există mai multe după publicitate;)

Cenușa de sodiu este mai bine cunoscută sub numele de sodă sau sodă, fiind utilizată la fabricarea săpunurilor, coloranților, medicamentelor, hârtiei și la tratarea apei din piscină. Dar aplicația sa principală este cu carbonatul de calciu și nisipul la fabricarea sticlei.
Calciul este familia 2, având tendința de a pierde doi electroni. Astfel, un atom de calciu se leagă de un radical carbonat:

Carbonatul de calciu este prezent în calcar și marmură. La stalactite și stalagmite care există în peșteri sunt constituite din acest carbonat; scoici, recife de corali și coji de ouă. Când văruim pereții, trunchiurile copacilor și alte locuri, folosim hidroxid de calciu (Ca (OH)2), care în timp reacționează cu dioxidul de carbon atmosferic pentru a forma carbonat de calciu.

Carbonatele sunt foarte frecvente la suprafața pământului, ca în cazul mineralelor. Reticulul său cristalin se poate rearanja în spațiu în două moduri: ortorombic (cum este cazul cu aragonitul mineral prezentat mai sus împreună cu formula carbonatului de calciu) și romboedru sau trigonal, cum este cazul calcitului (un alt mineral format din carbonat de calciu).
Carbonatii reactioneaza in prezenta acizilor, eliberand CO2, care se vede ușor printr-o efervescență.
De Jennifer Fogaça
Absolvent în chimie
Doriți să faceți referire la acest text într-o școală sau într-o lucrare academică? Uite:
FOGAÇA, Jennifer Rocha Vargas. „Carbonati”; Școala din Brazilia. Disponibil in: https://brasilescola.uol.com.br/quimica/carbonatos.htm. Accesat la 28 iunie 2021.
Chimie

Carbonat de sodiu, metoda Leblanc, metoda Ernest Solvay, sodă, sodă, fabricarea obișnuită a sticlei, tratarea apei pentru piscine, controlul pH-ului apei, tratarea textilelor, aditiv alimentar.
Chimie

Săruri zilnice, carbonat de calciu, clorură de sodiu, fluorură de sodiu, azotat de potasiu, azotat de sodiu sodiu, carbonat de sodiu, bicarbonat de sodiu, bicarbonat de sodiu, sulfit de sodiu, salpetru, sifon.


