Tu aldehide si cetone sunt funcții organice foarte asemănătoare. Ambele au în structura lor gruparea funcțională carbonil (C = O), cu singura diferență că, în cazul aldehide, apare întotdeauna la capătul lanțului de carbon, adică unul dintre liganzii carbonil carbon este hidrogen; cetonele au carbonilul între alți doi atomi de carbon.
Grupul funcțional aldehidelor:Grup funcțional de cetone:
O O
║ ║
C C ─ H C C ─ C
Din acest motiv, există cazuri de izomerism funcțional între aldehide și cetone. De exemplu, mai jos prezentăm doi izomeri funcționali care au aceeași formulă moleculară (C3H6O), dar una este o aldehidă (propanal), iar cealaltă este o cetonă (propanonă). Vedeți cum își schimbă total proprietățile și aplicațiile:
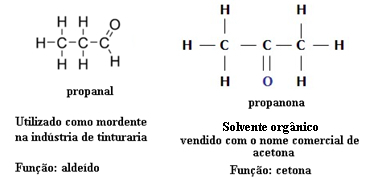
Exemplu de izomerism funcțional între aldehidă și cetonă
Imaginați-vă că vă aflați într-un laborator și găsiți un flacon cu un lichid incolor care are doar formula moleculară C3H6O. Ce ați face pentru a afla dacă este o cetonă sau o aldehidă?
Pentru a rezolva astfel de probleme,
există metode de diferențiere a aldehidelor și cetonelor pe baza reacției acestor compuși împotriva agenților de oxidare slabi. Așa cum se arată mai jos, când se confruntă cu oxidanți slabi, aldehidele reacționează prin oxidare, în timp ce cetonele nu reacționează. Spunem astaaldehidele acționează ca agenți reducători, dar cetonele nu, reacționează doar ca agenți reducători în contact cu oxidanții energetici.Aldehide + Oxidanți slabi → acid carboxilic
O O
║ ║
C ─ C ─ H + [O] → C ─ C ─ OH
Cetone + Oxidanți slabi → Nu reacționați
O
║
C ─ C ─ C + [O] → Nu apare nicio reacție
Pe această bază, este suficient să se efectueze această reacție și să se vadă dacă compusul reacționează sau nu. Dacă reacționează, știm că este o aldehidă; dacă nu reacționează, este o cetonă.
În plus, produsele formate în aceste reacții de oxidare a aldehidei sunt destul de vizibile, având loc modificări de culoare, așa cum se va arăta mai târziu.
Există trei metode principale de diferențiere a aldehidelor și cetonelor, care sunt:
1- Tollens reactiv: Acest reactiv este un soluție de amoniac de azotat de argint, adică conține azotat de argint (AgNO3) și hidroxid de amoniu în exces (NH4OH):
AgNO3 + 3 NH4OH → Ag (NH3)OH + NH4LA3 + 2 H2O
Tollens Reactive (numit după chimistul german Bernhard Tollens (1841-1918))
Așa cum se explică în text Realizarea unei oglinzi de argint, când o aldehidă este pusă în contact cu reactivul Tollens, aceasta este oxidată la acidul carboxilic corespunzător, în timp ce ionii de argint sunt reduși la Ag0 (argint metalic). Dacă această reacție este efectuată, de exemplu, într-o eprubetă, acest argint metalic se va depune pe pereții tubului, rezultând formarea unui film numit oglinda argintie. Acest rezultat observat este foarte frumos și este utilizat în procesul de fabricare a oglinzilor industriale.
Reacția care are loc poate fi reprezentată după cum urmează:
O O
║ ║
R ─ C ─ H + H2O → R ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 H+ → 2 NH4+
O O
║║
R C ─ H + 2 Ag+ + 2 NH3 + H2O → R C ─ OH + 2 Ag0 + 2 NH4+
aldehidă Tollens reactivacid carboxilic argint metalic (oglindă argintie)
Pe de altă parte, dacă punem cetona să reacționeze cu reactivul Tollens, nu se va produce formarea argintului metalic, deoarece cetonele nu pot reduce ionii Ag.+.
2- Reactiv Fehling: Acest reactiv este o soluție albastră de sulfat de cupru II (CuSO4) într-un mediu bazic, deoarece este amestecat cu o altă soluție formată din hidroxid de sodiu (NaOH) și tartrat de sodiu și potasiu (NaOOC-CHOH-CHOH-COOK). La soluția de sulfat de cupru II se adaugă tartrat pentru a-l stabiliza și a preveni precipitarea acestuia.
CUSO4 + 2 NaOH → Na2NUMAI4 + Cu (OH)2
Fehling Reactive (numit după chimistul german Hermann von Fehling (1812-1885))
În contact cu reactivul lui Fehling, o aldehidă formează acidul carboxilic prin oxidare, în timp ce ionii de cupru (Cu)2+) prezente în mijloc sunt reduse, formând un precipitat maroniu-roșcat (mai asemănător cărămizii), care este oxid cupros. Cetonele, pe de altă parte, nu reacționează - deoarece nu pot reduce ionii de Cu2+.
O O
║ ║
R ─ C ─ H + 2 Cu (OH)2 → R ─ C ─ OH + Cur2O + 2 H2O
aldehidă precipitat brun-roșcat
3- Reactivul lui Benedict: Acest reactiv este, de asemenea, format dintr-o soluție de sulfat de cupru II (Cu (OH)2) într-un mediu bazic, dar este amestecat cu citrat de sodiu.
Ca și în cazul reactivului Fehling, în cazul reacției dintre aldehidă și reactivul lui Benedict, există și ioni de cupru (Cu2+) prezente în mediu care sunt reduse și formează oxid cupros roșu.
Acest reactiv este utilizat pe scară largă în teste pentru a detecta prezența și conținutul de glucoză în urină. Glucoza are o structură aldehidă în structura sa, astfel încât reacționează cu reactivul lui Benedict prezent în benzi pentru aceste teste. De acolo, trebuie doar să comparați culoarea panglicii cu culoarea cântarului de pe ambalajul produsului.

Reactivul lui Benedict este utilizat pentru a determina conținutul de glucoză din urină.
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm

