Capacitatea conexiunilor de a atrage sarcini electrice este definită ca polaritate, care capătă un caracter diferit în funcție de conexiunea în care este prezentă.
În ceea ce privește legătura ionică și covalentă, aceasta din urmă face molecula nepolară. Molecula în care legătura ionică este responsabilă pentru menținerea atomilor împreună are polaritate.
Legătura predominantă dintre compușii organici este covalentă, astfel încât aceștia devin în principal compuși nepolari. Lanțurile lungi de carbon prezente în substanțele organice nu le permit alt caracter decât non-polaritatea.
Explicația vine din faptul că conexiunea are loc între elemente egale (Ç-Ç), de aceea au aceeași scară de electronegativitate. Vezi un exemplu:

molecula nepolare
Butanul reprezentat de structura de mai sus este un gaz, rețineți că atomii de legătură sunt aceiași (4 carboni legați împreună).
Dar nu înseamnă că fiecare compus organic este nepolar, prezența altor atomi între carboni conferă moleculei un caracter polar. Consultați exemplul:
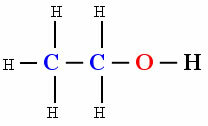
moleculă polară
Prezența hidroxilului Oh (Oxigenul legat de hidrogen) a făcut ca molecula compusului organic Etanol să arate polaritate.
Butanul este folosit ca gaz pentru brichete, iar etanolul este așa-numitul alcool obișnuit.
De Líria Alves
Absolvent în chimie
Echipa școlii din Brazilia
Vezi mai mult!
Proprietățile compușilor organici
Polaritate – Aflați de ce electronegativitatea influențează polaritatea unui apel.
Polaritatea legăturilor ionice și covalente
Chimie organica - Chimie - Școala din Brazilia
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/polaridade-dos-compostos-organicos.htm

